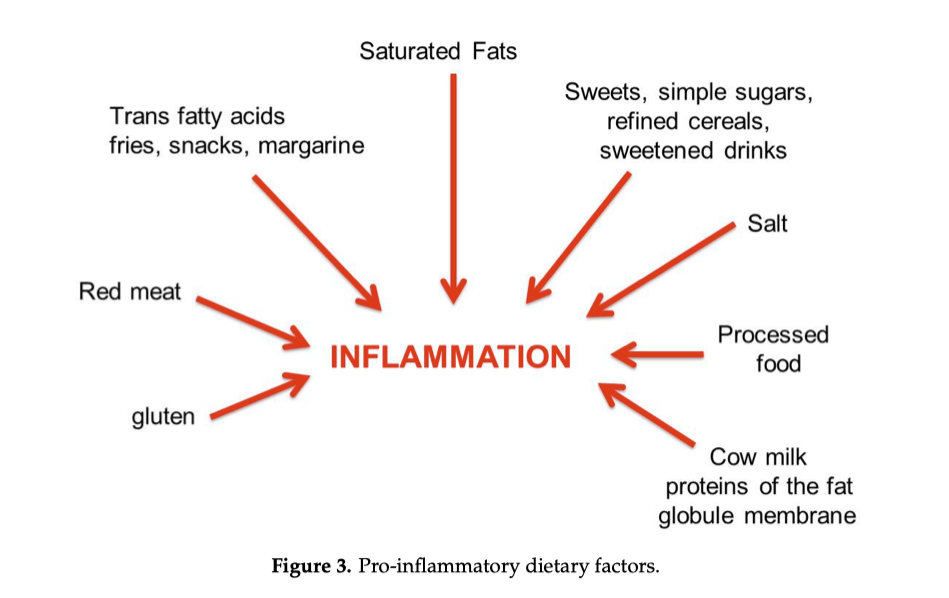
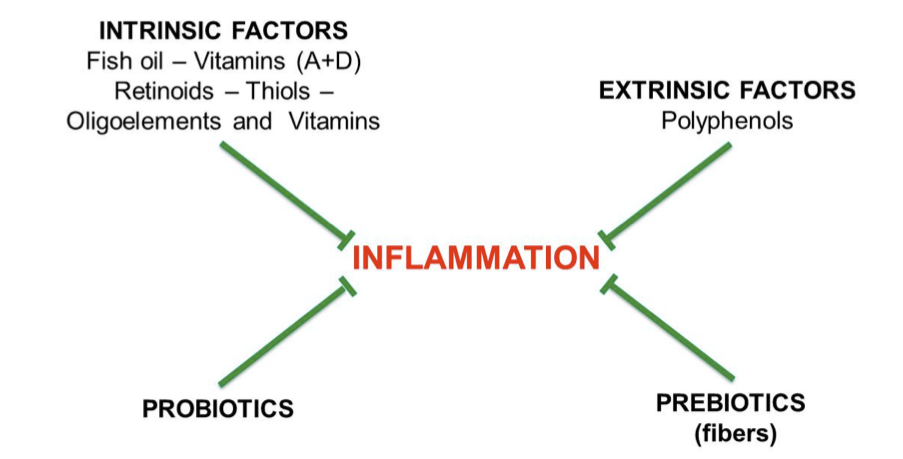
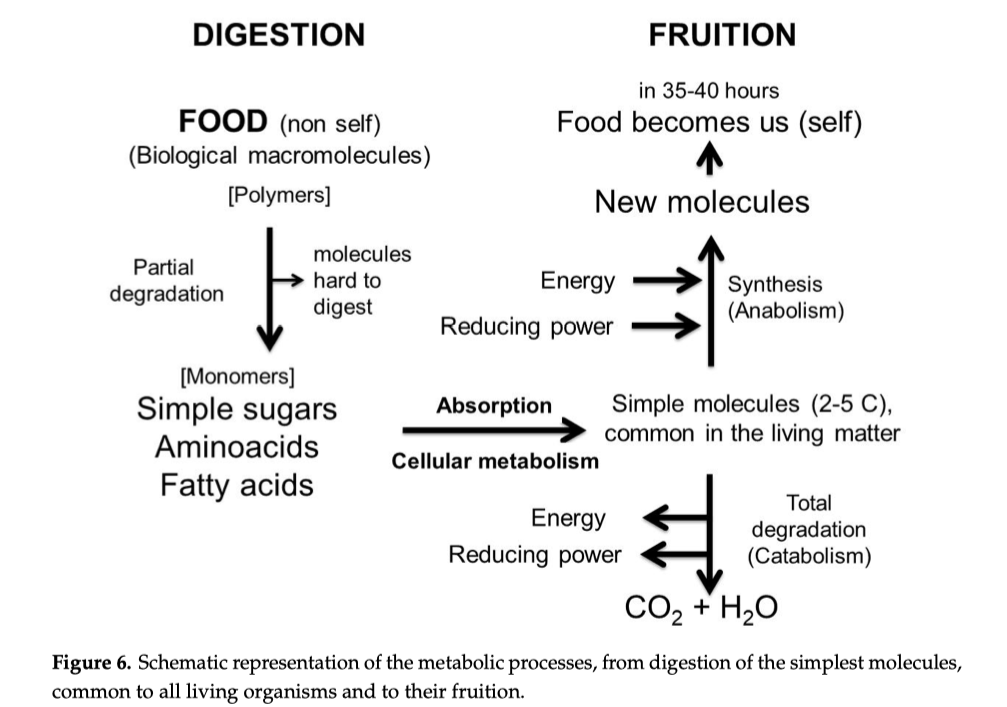
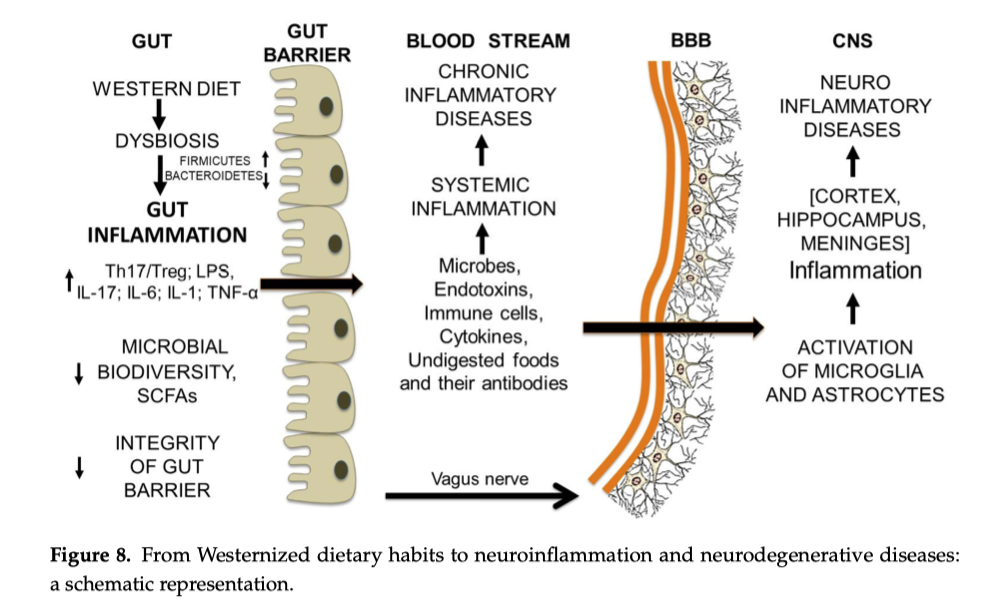
Questo vademecum raccoglie indicazioni pratiche di carattere alimentare e comportamentale utili a ridurre i fattori che possono favorire uno stato di infiammazione cronica di basso grado.
Per infiammazione cronica di basso grado si intende una condizione infiammatoria lieve ma persistente dell’organismo, spesso poco evidente o poco percepita. A differenza dell’infiammazione acuta — che è intensa, visibile e temporanea (come nel caso di un’infezione, di una ferita o di una malattia) — questa forma è più silenziosa e può protrarsi nel tempo. Negli ultimi anni numerosi studi hanno evidenziato come tale stato infiammatorio possa contribuire allo sviluppo o al peggioramento di diverse condizioni metaboliche e immunitarie.
Premessa
La dieta proposta è un insieme di accorgimenti e regole alimentari finalizzate a mantenere il microbiota intestinale in equilibrio e a favorire il miglior funzionamento possibile del sistema immunitario.
Per raggiungere questo obiettivo è utile ridurre o eliminare i fattori che possono alterare l’equilibrio del microbiota intestinale e interferire con l’efficienza del sistema immunitario.
Il microbiota è naturalmente dinamico: una certa variabilità è fisiologica e può dipendere, ad esempio, da cambiamenti nella dieta, nello stile di vita o nell’ambiente. A queste variazioni il microbiota può adattarsi in modo fisiologico oppure sviluppare risposte meno favorevoli.
Non tutte le variazioni del microbiota sono quindi negative. Tuttavia, quando tali cambiamenti determinano squilibri persistenti dell’ecosistema intestinale, possono favorire condizioni di alterazione del microbiota e contribuire all’insorgenza di infiammazione cronica di basso grado.
Ridurre questa condizione è quindi uno degli obiettivi principali del percorso.
Anche in presenza di patologie in atto, adottare indicazioni alimentari e comportamentali utili a ridurre l’infiammazione cronica di basso grado può contribuire a non aggravare ulteriormente il quadro clinico e a favorire un migliore equilibrio generale dell’organismo.
La dieta dovrebbe essere accompagnata anche da alcune regole di stile di vita, in particolare riguardo a:
-
gestione dello stress e dell’ansia
-
attività fisica regolare
-
abitudini di vita equilibrate
Questo aspetto non è affatto marginale. I numerosi studi sull’asse intestino–cervello hanno infatti evidenziato una stretta relazione bidirezionale tra sistema nervoso, intestino e microbiota.
Di conseguenza, condizioni di stress prolungato possono influenzare negativamente l’equilibrio intestinale e compromettere, almeno in parte o completamente, gli effetti positivi di una dieta corretta ed efficace.
Infine, ma non meno importante, va ricordato che la grande variabilità delle condizioni psicofisiche individuali e l’eterogeneità delle risposte a cure, trattamenti e regimi alimentari richiedono spesso una personalizzazione attenta della dieta, possibilmente supportata dal proprio medico o da uno specialista.
Va subito sottolineato che:
In un soggetto realmente sano*, il sistema immunitario e gli organi deputati alla regolazione dell’omeostasi sono fisiologicamente in grado di mantenere lo stato di salute e di difendere l’organismo dagli agenti esterni, inclusi quelli di origine alimentare. Questo equilibrio dipende dalla capacità dell’organismo di modulare in modo appropriato le risposte infiammatorie, preservare l’integrità della barriera intestinale e mantenere una comunicazione efficiente tra intestino, sistema immunitario e sistema nervoso.
Il metodo: cosa evitare e perché
-
Assumere troppo cibo: lo stomaco dovrebbe essere messo in grado di lavorare (digerire) al meglio. Meglio mangiare più volte che fare un unico pasto abbondante. La letteratura scientifica più recente suggerisce che la presenza di cibo non completamente digerito nel lume intestinale possa contribuire, in specifici contesti [1], a processi di infiammazione cronica di basso grado e a un aumento della permeabilità intestinale. “Per ‘specifici contesti’ si intende la concomitanza di una barriera gastrica inefficiente (ipocloridria), un rallentamento del transito (stasi) e un’alterazione della permeabilità intestinale (leaky gut), che trasformano i residui alimentari indigeriti in stimoli pro-infiammatori per il sistema immunitario.”
-
Pasti composti da pietanze differenti [2]: Più semplice è la composizione di un pasto più facile risulterà la digestione gastrica. La presenza di grassi [2.1], se significativa può rallentare il passaggio all’intestino prolungando la digestione con possibili effetti di “pesantezza” e gonfiore. Gli zuccheri semplici vengono digeriti molto velocemente, solitamente nell’intestino tenue. Se però li mangi dopo un pasto completo (magari ricco di proteine e fibre), rimangono “bloccati” nello stomaco [2.3] in attesa che il resto del cibo venga processato e possono fermentare [3].
-
Preparati industriali [4]: meno possibile; contengono additivi che, se assunti singolarmente una volta ogni tanto non creano problemi ma, se assommati tra loro, possono avere un’azione pro-infiammatoria più o meno marcata in relazione allo stato di salute del soggetto. In sintesi non è necessario eliminare rigidamente ogni alimento contenente additivi, ma privilegiare una dieta basata su alimenti poco processati riduce l’esposizione complessiva a miscele di additivi e rappresenta una strategia semplice, sicura e potenzialmente benefica per la salute intestinale e sistemica.
-
Bevande industriali: meno possibile ;generalmente contengono molto zucchero/edulcoranti/additivi.
-
Cibi per celiaci: il meno possibile quando non vi sia una reale necessità medica. Molti prodotti industriali senza glutine possono contenere quantità elevate di zuccheri, grassi e additivi, oltre ad avere spesso un contenuto di fibre inferiore rispetto ai prodotti tradizionali. Per questo motivo è preferibile limitarne il consumo quando non strettamente necessario. Va ricordato, inoltre, che gli additivi contenuti in questi prodotti, se sommati tra loro, possono avere un’azione pro-infiammatoria in relazione allo stato di salute del soggetto.
-
Vino/birra: con molta moderazione, perché l’alcol può interferire con il metabolismo epatico, aumentare l’apporto calorico e, se consumato frequentemente, favorire processi infiammatori e alterazioni dell’equilibrio intestinale.
-
Alcolici: no se non in casi saltuari.
-
Caffe: sì, in quantità compatibile con la tolleranza individuale alla caffeina, ma con attenzione all’eventuale contenuto complessivo di zucchero.
-
Spezie: sì, privilegiando quelle con proprietà digestive e antiossidanti (curcuma, zenzero, cannella, cumino) e usando con maggiore moderazione quelle più irritanti (pepe, peperoncino).
-
Fritti: con moderazione perché la frittura aumenta il contenuto calorico degli alimenti e può produrre composti ossidati e sostanze irritanti che, se consumati frequentemente, possono favorire processi infiammatori e affaticare la digestione.
-
Fibre: sono indispensabili. Possibilmente 3–4 volte al giorno. Le fibre rappresentano la principale e più importante fonte di nutrimento del microbiota: con esse il microbiota produce acidi grassi a catena corta (butirrato, acecato, propinato) utili alla salute intestinale.
-
Insaccati: con parsimonia, perché contengono generalmente quantità elevate di sale, conservanti (nitriti e nitrati) e grassi, elementi che se consumati frequentemente possono favorire processi infiammatori e squilibri metabolici.
-
Formaggi: sì, nella misura compatibile con il soggetto (pochi se intolleranti al lattosio o alla caseina). Non vanno eliminati completamente quando ben tollerati, perché rappresentano una buona fonte di proteine, calcio e altri micronutrienti utili all’organismo. È comunque preferibile privilegiare formaggi semplici e di buona qualità, consumati con moderazione.
-
Dolci: nella quantità compatibile con il soggetto. Se vi sono problemi con gli zuccheri (per peso o per glicemia) vanno assunti nelle dosi opportune per evitare squilibri. Non dimentichiamo però che rappresentano anche una fonte di piacere compensativo in molti stati di stress o ansia: moderazione sì, ma senza eliminarli completamente.
-
Glutine [5][5.1]: se possibile pasta integrale/semintegrale; pane: se possibile semintegrale/integrale di grano duro/farro dicocco o monococco. Il grano tenero contiene una componente del glutine molto difficile da digerire (33mer). Se possibile inserire più possibile prodotti realizzati con grani con glutine meno forte e più tollerabile (diversi grani antichi hanno queste caratteristiche).
-
Intolleranza al glutine non celiaca (NCGS). L’intolleranza di questo tipo è “dose dipendente”. Una volta accertato che si è intolleranti ma non celiaci è necessario individuare qual è la quantità che è tollerabile senza avere problemi. In questi casi i prodotti realizzati con grani con glutine meno tenace e più tollerabile (diversi grani antichi hanno queste caratteristiche) possono aiutare ad affrontare meglio il problema. Va inoltre sottolineato che molti prodotti per celiaci contengono diversi additivi: per questo aspetto si richiama quanto detto al punto 3 e nella nota [4]
-
Acqua: bere regolarmente durante la giornata in quantità adeguata. L’acqua è indispensabile per il corretto funzionamento del metabolismo, della digestione e dei processi di eliminazione delle scorie. (I mecici ci perseguitano…1,5 – 2 litri….)
-
The verde perché: contiene polifenoli e sostanze antiossidanti che possono contribuire alla protezione cellulare e all’equilibrio metabolico.
-
Medicine: solo se veramente necessarie e su prescrizione medica.
-
Integratori: da utilizzare consultando uno specialista per definire un’assunzione “personalizzata” in funzione del disturbo/patologia presente. Inoltre molti non sono sufficientemente testati su popolazioni ampie e ben caratterizzate.
Comportamenti specifici :
-
Fare attività fisica anche solo moderatamente.
-
Se in attività lavorativa evitare che questa porti a stress.
-
Se in periodo post attività lavorativa impegnarsi in attività che richiedano concentrazione e, se possibile, creatività. Realizzare progetti è altamente utile per mantenere in attività le funzioni cognitive.
-
Non fumare
-
Con il proprio medico definire gli accertamenti generali di routine necessari per un buon monitoraggio della propria salute oltre ad accertamenti specifici per situazioni mediche già accertate.
* È infine opportuno precisare che il concetto di “soggetto sano” non coincide semplicemente con l’assenza di malattie clinicamente diagnosticate. In senso fisiologico più rigoroso, una persona può essere definita realmente sana quando non presenta patologie in atto e non si trova in uno stato di infiammazione cronica di basso grado. Questa distinzione è tutt’altro che marginale, poiché nella pratica clinica il termine “sano” viene spesso utilizzato in senso riduttivo, coincidente con la sola assenza di diagnosi formali.
Note:
[1] Cibo indigerito
L’infiammazione di basso grado non è causata dal cibo in sé, ma dalla rottura dell’equilibrio tra digestione, microbiota e barriera intestinale. In particolare:
-
Il fallimento enzimatico e acido: Se lo stomaco (per stress o farmaci) non degrada le proteine in piccoli aminoacidi, restano catene peptidiche lunghe che il corpo può scambiare per minacce.
-
La trasformazione biochimica: I residui indigeriti, ristagnando, subiscono processi di putrefazione (proteine) o fermentazione eccessiva (zuccheri), producendo metaboliti tossici (ammoniaca, fenoli, gas) che irritano la mucosa.
-
La breccia immunitaria: In presenza di una mucosa intestinale “permeabile”, queste macromolecole e tossine superano la parete cellulare ed entrano in contatto diretto con il sistema immunitario, mantenendolo in uno stato di allerta perenne (rilascio di citochine infiammatorie).
[2] La semplicità e il “carico” enzimatico
Ogni macronutriente (carboidrati, proteine, grassi) richiede enzimi e tempi di scomposizione diversi. Quando mescoliamo troppe pietanze differenti:
-
Lo stomaco deve gestire un mix chimico complesso.
-
Il corpo fatica a ottimizzare il pH gastrico per ogni alimento.
-
Risultato: Una digestione più rapida e “pulita” avviene quando i pasti sono composti da pochi ingredienti ben abbinati.
[2.1] Il ruolo dei grassi
I grassi sono i nutrienti più lenti da digerire. La loro presenza invia segnali ormonali (come la colecistochina) che dicono allo stomaco di rallentare lo svuotamento verso il duodeno.
-
Il lato positivo: Donano un senso di sazietà prolungato.
-
Il lato negativo: Se il pasto è eccessivamente grasso, il cibo ristagna nello stomaco. Questo processo di fermentazione o ristagno è ciò che causa quella sensazione di “mattone sullo stomaco” e il gonfiore addominale.
[2.3] Consigli per un pasto bilanciato ma leggero
Per evitare la pesantezza senza rinunciare al gusto, potresti seguire queste piccole accortezze:
-
Preferire cotture semplici: Vapore, piastra o forno piuttosto che fritture o soffritti prolungati.
-
Limitare le proteine diverse: Evitare di mischiare nello stesso pasto uova, formaggi e carne.
-
Grassi a crudo: Usare l’olio extravergine d’oliva a fine cottura per mantenerne intatte le proprietà e facilitarne la scomposizione.
In sintesi: Meno “ostacoli” diamo al nostro apparato digerente sotto forma di combinazioni complesse e grassi pesanti, più energia avremo a disposizione dopo il pasto invece di sentirci assonnati e gonfi.
[3] Zuccheri
Mentre i grassi rallentano la digestione per una questione di “gestione biochimica” (lo stomaco chiude la valvola per prendersi tempo), gli zuccheri semplici a fine pasto (la quantità qui gioca un ruolo importante) creano una sorta di “coda digestiva” nello stomaco.
3.1. L’effetto “Tappo” e la Fermentazione
Gli zuccheri semplici vengono digeriti molto velocemente, solitamente nell’intestino tenue. Inseriti dopo un pasto completo (magari ricco di proteine e fibre), rimangono “bloccati” nello stomaco in attesa che il resto del cibo venga processato.
-
Conseguenza: In quell’ambiente caldo e umido, gli zuccheri iniziano a fermentare.
-
Risultato: Produzione di gas, gonfiore addominale immediato e senso di acidità.
3.2. Il richiamo di liquidi (Osmosi)
Gli zuccheri sono sostanze “osmotiche”, ovvero richiamano acqua all’interno dello stomaco e dell’intestino per essere diluiti.
-
Questo afflusso di liquidi può causare una sensazione di distensione addominale e, in alcuni casi, crampi o transito accelerato (ma non nel senso buono del termine).
3.3. L’impatto sull’insulina
A differenza dei grassi, che non stimolano significativamente l’insulina, il dolce a fine pasto (la quantità qui gioca un ruolo importante) può causare un picco glicemico importante.
-
Se il pasto precedente era già ricco di carboidrati (pasta o pane), il dolce è la “goccia che fa traboccare il vaso”.
-
Questo picco è spesso seguito da un crollo (ipoglicemia reattiva) che ti fa sentire stanco e privo di energie poco dopo aver mangiato
|
Caratteristica |
Grassi Abbondanti |
Zuccheri (Dolce) |
|
Azione principale |
Rallentano lo svuotamento gastrico. |
Fermentano in attesa di essere digeriti. |
|
Sensazione |
Pesantezza, “pietra nello stomaco”. |
Gonfiore, aria nella pancia, sonnolenza. |
|
Effetto Ormonale |
Senso di sazietà prolungato. |
Picco di insulina e successiva stanchezza. |
3.4. Fermentazione nello stomaco
3.4.1. Condizioni Normali: La Barriera Acida
In un soggetto realmente sano*, la fermentazione nello stomaco è pressoché assente perché è un ambiente molto acido dovuto all’acido cloridico.
Ambiente ostile:
Lo stomaco secerne acido cloridrico, mantenendo un pH molto basso (circa 1,5–3,0). Questo elevato grado di acidità agisce come un vero e proprio filtro di sicurezza, neutralizzando la maggior parte dei batteri e dei lieviti ingeriti con il cibo.
Velocità di transito:
In condizioni normali, gli zuccheri semplici passano rapidamente nel duodeno (circa 15–30 minuti), senza lasciare ai pochi microrganismi sopravvissuti il tempo necessario per avviare processi fermentativi.
Lo stomaco, tuttavia, non è completamente sterile. Alcuni microrganismi possono, in determinate circostanze, essere presenti e svolgere un ruolo limitato:
Lieviti (come Candida albicans):
Sono naturalmente presenti nel tratto digestivo. Se gli zuccheri rimangono nello stomaco troppo a lungo, ad esempio a causa di un pasto precedente lento da digerire, i lieviti possono metabolizzarli producendo gas (anidride carbonica) e piccole quantità di etanolo.
Batteri acido-tolleranti:
Alcuni ceppi di lattobacilli o batteri provenienti dal duodeno (specialmente quando l’acidità gastrica è temporaneamente tamponata dal cibo) possono contribuire a processi fermentativi limitati.
3.4.2. Condizioni Alterate: quando lo Stomaco “Fermenta”
La fermentazione diventa possibile quando la barriera acida si riduce oppure il cibo ristagna nello stomaco. Le cause principali possono essere:
Stress cronico (asse cervello-intestino):
Lo stress prolungato può agire su due fronti:
-
Riduzione della secrezione acida: attraverso l’attivazione del sistema nervoso simpatico, lo stress può diminuire la produzione di HCl, aumentando il pH gastrico e rendendo l’ambiente più favorevole alla sopravvivenza dei microbi.
-
Alterazione della motilità: lo stress può modificare le contrazioni gastriche, rallentando lo svuotamento dello stomaco.
Pasti molto complessi o ricchi di grassi:
I grassi stimolano segnali ormonali che rallentano lo svuotamento gastrico e la apertura del piloro. Se sopra questo rallentamento vengono introdotti zuccheri semplici, il contenuto gastrico può permanere più a lungo nello stomaco.
Uso di farmaci:
Gli inibitori di pompa protonica (PPI) aumentano artificialmente il pH gastrico, riducendo l’effetto battericida naturale dell’acido cloridrico.
Presenza eccessiva di lieviti (SIFO):
In condizioni di disbiosi, lieviti come Saccharomyces o Candida possono colonizzare maggiormente il tratto digestivo superiore e contribuire alla fermentazione degli zuccheri.
3.4.3. Le Conseguenze: cosa provoca la Fermentazione Gastrica
Anche se numericamente inferiore a quella intestinale, la fermentazione nello stomaco è molto fastidiosa perché avviene in un organo posto in alto nel tronco:
-
Produzione di Gas ($CO_2$): Il gas si accumula rapidamente, causando la distensione delle pareti gastriche (senso di palloncino sotto lo sterno).
-
Eruttazioni e Reflusso: La pressione del gas spinge contro il cardias (la valvola superiore). Questo può causare la risalita di aria mista a vapori acidi o cibo (reflusso).
-
Acidità Organica: I batteri/lieviti producono acidi organici (come l’acido lattico) che irritano la mucosa, dando una sensazione di bruciore diversa da quella dell’acido cloridrico puro.
-
Sonnolenza Post-Prandiale: La produzione di piccole quantità di sottoprodotti della fermentazione (come l’etanolo o l’acetaldeide) può contribuire alla “nebbia mentale” o alla stanchezza estrema dopo aver mangiato dolci.
In sintesi
La fermentazione gastrica non rappresenta un processo fisiologico normale, ma può indicare un’alterazione dell’ambiente digestivo, dovuta a una riduzione dell’acidità gastrica o a un rallentamento dello svuotamento dello stomaco, condizioni che permettono ai microrganismi di metabolizzare gli zuccheri prima che avvenga una digestione completa.
[4] Additivi e Salute Intestinale
L’impatto degli additivi alimentari sulla salute non dipende solo dalla loro tossicità intrinseca (regolata dalle autorità sanitarie), ma dal loro effetto sinergico sulla barriera intestinale. In particolare, la ricerca evidenzia due meccanismi critici:
-
Alterazione del muco protettivo (Emulsionanti): Additivi come la carbossimetilcellulosa (E466) o il polisorbato 80 (E433), comuni in salse e dolci industriali, possono agire come tensioattivi. Essi tendono a “sciogliere” lo strato di muco che riveste l’intestino, permettendo ai batteri di entrare in contatto diretto con le cellule della mucosa, innescando così una risposta infiammatoria cronica.
-
Disbiosi e Permeabilità (Dolcificanti e Conservanti): L’assunzione costante di miscele di additivi può alterare la composizione del microbiota (disbiosi). Uno squilibrio batterico, unito all’azione di alcuni conservanti, può indebolire le “giunzioni serrate” (tight junctions) tra le cellule intestinali. Questo aumento della permeabilità (leaky gut) facilita il passaggio di frammenti batterici e molecole indigerite nel sangue, alimentando un’infiammazione sistemica di basso grado.
[5] Glutine indigerito
Negli individui sani, allo stato attuale delle conoscenze, non esistono evidenze cliniche solide e conclusive che dimostrino un impatto sistemico significativo del glutine sulla permeabilità intestinale o sull’equilibrio infiammatorio dell’organismo.
Ciò nonostante, nei soggetti che presentano predisposizioni genetiche, vulnerabilità immunologiche o condizioni cliniche già presenti — anche quando non ancora chiaramente manifeste sul piano clinico — l’adozione di un criterio di prudenza nutrizionale non rappresenta un eccesso di cautela, ma piuttosto un atteggiamento di responsabilità preventiva. Tale approccio non implica necessariamente l’eliminazione indiscriminata del glutine dalla dieta, bensì una valutazione attenta e personalizzata del contesto clinico, metabolico e nutrizionale della persona.
In questi casi l’alimentazione può infatti contribuire, in senso positivo o negativo, alla modulazione dell’equilibrio infiammatorio e immunitario dell’organismo, all’interno di una visione sistemica della salute.
La qualità dell’alimentazione quotidiana non esercita effetti esclusivamente sull’intestino. Essa influenza il tono immunitario generale, il livello di infiammazione cronica di basso grado e, indirettamente, anche la salute cerebrale attraverso i complessi meccanismi dell’asse intestino–cervello. Prendersi cura dell’intestino significa quindi, in larga misura, prendersi cura dell’intero organismo.
[5.1] Glutine e permeabilità intestinale. Il glutine è una proteina complessa ricca di prolamine (gliadine) che il nostro sistema enzimatico non riesce a digerire completamente.
Le gliadine sono infatti costituite da lunghe catene di aminoacidi — i “mattoncini” delle proteine — legati tra loro in modo tale da rendere difficile l’azione degli enzimi digestivi, che non riescono a separare completamente questi aminoacidi prima dell’assorbimento da parte della parete intestinale.
In soggetti predisposti, alcuni di questi frammenti proteici non completamente digeriti possono stimolare il rilascio di zonulina, una proteina che agisce come regolatore delle giunzioni intestinali.
Mentre in un individuo sano queste “porte” si richiudono rapidamente senza conseguenze, nei soggetti vulnerabili possono rimanere aperte più a lungo, facilitando il fenomeno della permeabilità intestinale e la comparsa di processi infiammatori di basso grado, come descritto nei punti precedenti.
Riferimenti scientifici principali
Di seguito sono riportati alcuni studi scientifici di alto profilo che supportano i concetti descritti nel vademecum, in particolare riguardo alla permeabilità intestinale e al possibile impatto degli additivi alimentari ed emulsionanti sull’equilibrio intestinale.
1. Sulla Permeabilità Intestinale e Zonulina (Punti [1] e [5])
Questa ricerca è fondamentale perché ha identificato il meccanismo biologico attraverso cui il glutine e la salute intestinale interagiscono, introducendo il concetto di “apertura” delle giunzioni serrate.
-
Autore: Fasano, A.
-
Titolo: Zonulin, regulation of tight junctions, and autoimmune diseases.
-
Anno: 2011 (con aggiornamenti continui fino al 2020)
-
Abstract Esteso:
La ricerca descrive la scoperta della zonulina, uno dei principali modulatori fisiologici delle giunzioni serrate intestinali (tight junctions). Lo studio dimostra come frammenti indigeriti di glutine (gliadina) stimolino il rilascio di zonulina non solo in soggetti celiaci, ma anche in individui con predisposizione genetica. Questo rilascio provoca un aumento della permeabilità intestinale, permettendo il passaggio di antigeni dal lume intestinale al flusso sanguigno. Il lavoro evidenzia come questo processo sia alla base dell’infiammazione cronica di basso grado e possa innescare risposte immunitarie sistemiche, contribuendo alla comprensione scientifica del fenomeno della permeabilità intestinale.
2. Sull’effetto degli Emulsionanti e muco intestinale (Punto [4])
Questo studio è una pietra miliare per quanto riguarda i “preparati industriali” e spiega perché l’effetto cumulativo degli additivi è preoccupante per il microbiota.
-
Autore: Chassaing, B., et al.
-
Titolo: Dietary emulsifiers impact the mouse gut microbiota promoting colitis and metabolic syndrome.
-
Anno: 2015 (pubblicato su Nature, una delle riviste più prestigiose al mondo)
-
DOI: 10.1038/nature14232
-
Abstract Esteso:
Gli autori hanno analizzato l’impatto di due comuni emulsionanti industriali: la carbossimetilcellulosa e il polisorbato 80. Lo studio dimostra che queste sostanze non sono inerti, ma alterano direttamente la composizione del microbiota e l’interazione tra batteri e ospite. In particolare, gli emulsionanti riducono lo spessore del muco protettivo intestinale, permettendo ai batteri di avvicinarsi eccessivamente alle cellule epiteliali. Ciò causa un’infiammazione cronica intestinale che si riflette a livello sistemico con alterazioni metaboliche (aumento della glicemia e dell’adiposità). La ricerca suggerisce che l’ampio uso di questi additivi possa aver contribuito all’aumento globale delle malattie infiammatorie croniche.
Perché citare queste ricerche nel Vademecum?
-
Validazione del “leaky gut”: La ricerca di Fasano toglie il concetto di “permeabilità intestinale” dall’ambito della medicina alternativa, portandolo nella medicina accademica.
-
Pericolo degli Ultra-Processati: Lo studio di Chassaing su Nature fornisce una prova biochimica del perché non è solo lo zucchero il problema dei cibi industriali, ma la loro struttura chimica (emulsionanti).
-
Approccio Sistemico: Entrambi gli studi confermano che ciò che accade nell’intestino ha riflessi immediati sul metabolismo e sul sistema immunitario generale (infiammazione di basso grado).
Conclusione
Prendersi cura dell’intestino significa adottare un atteggiamento di prevenzione consapevole. Non è necessaria una rigidità assoluta, ma una scelta alimentare semplice, equilibrata e di qualità, capace di proteggere non solo l’intestino, ma l’intero organismo e anche la salute del cervello.
Infiammazione cronica di basso grado nella divulgazione scientifica italiana (2025-2026)
Introduzione alle fonti giornalistiche
Selezione di articoli italiani autorevoli del 2025-2026 che trattano in modo diretto o sostanziale l’infiammazione cronica di basso grado, soprattutto in rapporto a longevità, dieta, attività fisica, stress e metabolismo. Tra i più pertinenti ci sono: “Infiammazione cronica silente: cos’è, sintomi e come curarla” di Style/Corriere della Sera del 10 aprile 2026; “È vero che lo sport non serve a dimagrire?…” di Corriere della Sera del 21 marzo 2026; “Le tre ‘F’ che mantengono in salute l’intestino (e il cervello)” di Cook/Corriere del 14 marzo 2026; “Sì, la dieta può rallentare l’invecchiamento” di la Repubblica Salute dell’11 agosto 2025; “Il segreto della longevità per il 2026? Respira, riposa, sorridi e impara a perdonare” di la Repubblica Salute del 23 dicembre 2025; e “Dimmi come mangi e ti dirò come invecchi” di la Repubblica Salute del 30 dicembre 2025.
Di seguito viene presentato un abstract esteso costruito a partire da questi articoli.
Abstract esteso
Nel giornalismo scientifico e sanitario italiano del 2025-2026, l’infiammazione cronica di basso grado emerge come una chiave interpretativa trasversale per comprendere l’invecchiamento biologico e molte patologie cronico-degenerative. Gli articoli selezionati la descrivono non come un episodio acuto e visibile, ma come uno stato persistente, “silente”, di attivazione immunitaria a bassa intensità, spesso privo di sintomi specifici ma capace, nel tempo, di favorire insulino-resistenza, aumento del grasso addominale, stanchezza cronica e maggior rischio cardiovascolare e neurodegenerativo. Style/Corriere la definisce infatti un “nemico silente” e un “terreno comune” di numerose condizioni cliniche, sottolineando come venga spesso normalizzata nella vita quotidiana.
Una prima linea narrativa molto forte riguarda il rapporto tra infiammazione e invecchiamento. la Repubblica Salute collega esplicitamente l’infiammazione cronica di basso grado all’“inflammaging”, cioè a quel processo per cui l’organismo invecchia in presenza di una persistente attivazione immunitaria e di stress ossidativo. Nell’articolo sui telomeri, l’idea centrale è che il potenziale infiammatorio della dieta possa accelerare oppure rallentare l’erosione telomerica: gli alimenti pro-infiammatori vengono associati a telomeri più corti, mentre regimi alimentari più ricchi di fibre, polifenoli e grassi insaturi vengono presentati come plausibilmente protettivi. Lo stesso quotidiano, a fine 2025, ribadisce che prevenire l’infiammazione è essenziale per la longevità, perché questa accelera l’età biologica e aumenta il rischio delle principali malattie dell’età avanzata.
Una seconda area tematica riguarda la dieta come fattore di modulazione. Gli articoli non propongono soluzioni miracolistiche, ma convergono su alcuni elementi ricorrenti: ridurre cibi ultra-processati o ad alto carico infiammatorio, stabilizzare la glicemia, privilegiare alimenti poco processati, grassi di qualità, fibre e cibi che sostengano il microbiota intestinale. Style/Corriere elenca tra gli alimenti più favorevoli pesce ricco di omega-3, verdure a foglia verde, frutti di bosco, olio extravergine, semi oleosi, curcuma, zenzero e fermentati, insistendo però sul fatto che il beneficio dipende dal pattern alimentare complessivo e non dal singolo “superfood”. la Repubblica rafforza questa impostazione citando l’Indice Infiammatorio della Dieta (DII), usato per stimare quanto una dieta sia pro- o anti-infiammatoria.
Una terza direttrice è il ruolo del movimento fisico. Nel Corriere della Sera del 21 marzo 2026, l’attività fisica viene presentata come un “farmaco multi-target” che non serve soltanto a consumare calorie, ma agisce su sensibilità insulinica, grasso epatico, pressione, glicemia, sonno e umore. In questo quadro, il movimento e la dieta sana sono descritti come potenti modulatori dell’infiammazione cronica di basso grado, anche grazie alla produzione di miochine da parte del muscolo in contrazione, cioè molecole con effetti antinfiammatori e metabolici. L’articolo di Cook/Corriere sul microbiota completa il quadro suggerendo che sport regolare e salute delle mucose intestinali siano strettamente collegati, con possibili benefici combinati su autofagia, funzione immunitaria e riduzione dell’infiammazione sistemica.
Un quarto filone riguarda stress, sonno e regolazione neuroendocrina. Style/Corriere insiste sul fatto che stress cronico e cattiva qualità del sonno alimentano direttamente i processi infiammatori; vengono richiamati l’aumento del cortisolo, il peggioramento della sensibilità insulinica e l’aumento della fame come meccanismi che mantengono l’organismo in uno stato di allerta prolungato. Anche Wired Italia, pur non essendo centrato esclusivamente sull’infiammazione cronica di basso grado, rafforza l’idea che una disregolazione cronica del cortisolo e dei ritmi circadiani possa contribuire a obesità viscerale, alterazioni metaboliche e stress persistente, tutti elementi coerenti con il quadro pro-infiammatorio discusso dagli altri articoli. la Repubblica, nell’intervista sulla longevità, estende il ragionamento alla salute orale e al benessere psicologico, suggerendo che anche parodontopatie e stress emotivo cronico possano aumentare l’infiammazione sistemica.
Nel complesso, questi articoli presentano l’infiammazione cronica di basso grado come una condizione sistemica in cui convergono alimentazione, composizione corporea, stress, sonno, microbiota, esercizio fisico e invecchiamento cellulare. Il messaggio giornalistico prevalente è che non si tratti di una malattia unica, ma di un “substrato biologico” che può precedere o accompagnare molte malattie. Da qui deriva una visione fortemente preventiva: non spegnere un sintomo, ma ridurre il carico infiammatorio quotidiano attraverso interventi ripetuti e realistici sullo stile di vita.
Dal punto di vista critico, va però osservato che questi testi sono articoli di divulgazione giornalistica, non revisioni sistematiche o linee guida. Alcuni riportano studi o interviste a specialisti in modo corretto ma sintetico; altri usano toni più lifestyle e semplificano un quadro biologico complesso. La convergenza tra testate diverse, comunque, è notevole: tutte riconoscono l’infiammazione cronica di basso grado come un nodo centrale fra metabolismo e invecchiamento, e tutte indicano nelle abitudini di vita il principale spazio di intervento. Questa convergenza non sostituisce la prova clinica, ma segnala che il tema è ormai stabilmente entrato nel discorso pubblico italiano sulla prevenzione e sulla longevità.
Fonti giornalistiche
-
Style – Corriere della Sera, 10 aprile 2026, “Infiammazione cronica silente: cos’è, sintomi e come curarla”.
-
Corriere della Sera, 21 marzo 2026, “È vero che lo sport non serve a dimagrire? Ecco perché l’esercizio non conta solo per le calorie consumate”.
-
Cook – Corriere della Sera, 14 marzo 2026, “Le tre ‘F’ che mantengono in salute l’intestino (e il cervello)”.
-
la Repubblica – Salute, 11 agosto 2025, “Sì, la dieta può rallentare l’invecchiamento”.
-
la Repubblica – Salute, 23 dicembre 2025, “Il segreto della longevità per il 2026? Respira, riposa, sorridi e impara a perdonare”.
-
la Repubblica – Salute, 30 dicembre 2025, “Dimmi come mangi e ti dirò come invecchi”.
Approfondimento di alcuni articoli significativi
1. Corriere della Sera – Style
Corriere della Sera
Titolo: Infiammazione cronica silente: cos’è e come contrastarla con alimentazione e stile di vita
Sezione: Style – Benessere
Data: 10 aprile 2026
Breve citazione dall’articolo
“L’infiammazione cronica di basso grado è un processo silente che può favorire nel tempo malattie metaboliche, cardiovascolari e neurodegenerative.”
Abstract esteso
L’articolo descrive l’infiammazione cronica di basso grado come una condizione biologica persistente caratterizzata da una lieve ma continua attivazione del sistema immunitario. A differenza dell’infiammazione acuta, non presenta sintomi evidenti ma può svilupparsi lentamente nel tempo, contribuendo allo sviluppo di diverse patologie croniche. Tra queste vengono citate obesità, diabete di tipo 2, malattie cardiovascolari e processi di invecchiamento accelerato.
Il testo sottolinea il ruolo centrale dello stile di vita nella modulazione dei processi infiammatori. L’alimentazione ricca di alimenti ultra-processati, zuccheri raffinati e grassi saturi favorirebbe uno stato pro-infiammatorio, mentre una dieta equilibrata ricca di fibre, vegetali, pesce e grassi insaturi avrebbe effetti antinfiammatori. Viene inoltre evidenziato il contributo del microbiota intestinale nella regolazione della risposta immunitaria sistemica.
Un’altra dimensione rilevante riguarda il rapporto tra infiammazione cronica e invecchiamento biologico. L’articolo richiama il concetto di inflammaging, cioè l’invecchiamento accelerato associato a uno stato infiammatorio persistente. Secondo gli esperti citati, la riduzione del carico infiammatorio attraverso alimentazione equilibrata, attività fisica regolare, sonno adeguato e gestione dello stress rappresenta una strategia preventiva fondamentale.
2. la Repubblica – Salute
la Repubblica
Titolo: Sì, la dieta può rallentare l’invecchiamento: il ruolo dell’infiammazione e dei telomeri
Sezione: Salute
Data: 11 agosto 2025
Breve citazione
“Una dieta con alto indice infiammatorio è associata a telomeri più corti e a un invecchiamento biologico più rapido.”
Abstract esteso
L’articolo analizza il legame tra dieta, infiammazione sistemica e invecchiamento cellulare. Viene presentato il concetto di indice infiammatorio della dieta (Dietary Inflammatory Index), utilizzato in studi epidemiologici per valutare il potenziale pro- o anti-infiammatorio dell’alimentazione.
Secondo le ricerche citate, regimi alimentari ricchi di zuccheri semplici, grassi saturi e alimenti altamente processati sono associati a un aumento dei marcatori infiammatori e a una maggiore probabilità di telomeri più corti. I telomeri, strutture che proteggono le estremità dei cromosomi, rappresentano un indicatore biologico dell’invecchiamento cellulare.
Al contrario, una dieta ricca di frutta, verdura, fibre, cereali integrali, legumi e pesce appare correlata a un minor livello di infiammazione sistemica. L’articolo suggerisce che il modello alimentare mediterraneo possa rappresentare una strategia efficace per modulare i processi infiammatori cronici e favorire una maggiore longevità.
3. Corriere della Sera – Salute
Corriere della Sera
Titolo: È vero che lo sport non serve a dimagrire? Perché l’esercizio conta anche oltre le calorie
Data: 21 marzo 2026
Breve citazione
“L’attività fisica regolare riduce l’infiammazione sistemica e migliora sensibilità insulinica, pressione e metabolismo.”
Abstract esteso
L’articolo discute il ruolo dell’attività fisica nella salute metabolica e nella prevenzione delle malattie croniche. Il testo chiarisce che l’esercizio fisico non agisce soltanto attraverso il consumo calorico, ma produce una serie di effetti fisiologici complessi che includono la regolazione dei livelli di glucosio nel sangue, il miglioramento della sensibilità insulinica e la riduzione dei livelli di infiammazione sistemica.
Una parte dell’analisi riguarda la produzione di miochine, molecole rilasciate dal muscolo durante la contrazione che esercitano effetti antinfiammatori e metabolici. Attraverso questi meccanismi, l’attività fisica contribuisce alla riduzione dell’infiammazione cronica di basso grado e al miglioramento della salute cardiovascolare e metabolica.