Cibo non digerito e infiammazione intestinale -II parte- aggiornamento 24-02-2026
Note riassuntive – Punti salienti della ricerca
6. Dieta infiammatoria vs antinfiammatoria
Come mostrato nella Figura 3, la dieta occidentale, ad alto contenuto energetico, è tipicamente pro-infiammatoria, ricca di grassi animali saturi, carni rosse, patatine fritte, snack e margarine (acidi grassi trans), bevande zuccherate e zuccheri semplici, sale, cibi lavorati e condimenti elaborati. La dieta occidentale è spesso associata a uno stile di vita sedentario ed è caratterizzata dalla scarsità di fibre. Anche l’assunzione di alcol e il fumo sono pro-infiammatorie.
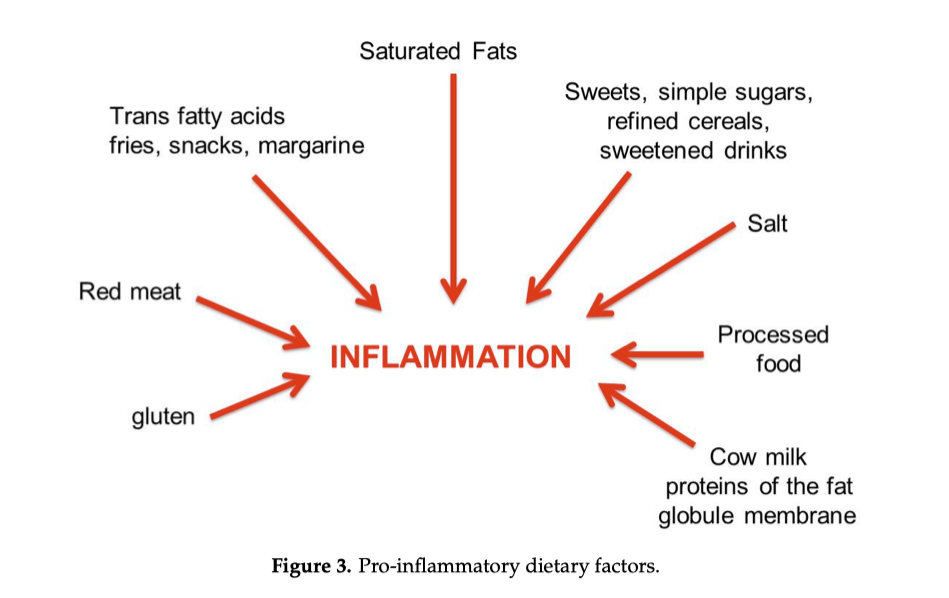
In sintesi:
Dieta pro-infiammatoria
-
carni rosse
-
grassi saturi
-
zuccheri semplici
-
alimenti ultra-processati
-
sedentarietà
-
alcol e fumo
Dieta antinfiammatoria
-
verdura
-
frutta
-
legumi
-
cereali integrali
-
pesce (omega-3)
-
olio extravergine di oliva
-
spezie
-
polifenoli
-
prebiotici e probiotici
Gli alimenti trasformati sono pro-infiammatori perché possono contenere diversi metalli chimici aggiunti, pesticidi, aromi artificiali, coloranti, erbicidi e conservanti, che hanno effetti deleteri sugli emulsionanti, antibiotici e, inoltre, metalli pesanti, microbiota e vitamine. Additivi: aromi artificiali, coloranti, conservanti, emulsionanti, antibiotici e, inoltre, alti livelli di vitamina D. Pesticidi ed erbicidi, che hanno effetti deleteri sul microbiota intestinale e sui livelli di vitamina D.
La Figura 4 mostra i fattori attivi della dieta antinfiammatoria, principalmente vegetariana e ricca di fibre. Questa dieta, dieta, che è intesa come essere povera di pane e caseinati, caseinati, si basa sull’assunzione di verdura, frutta, verdura. La Figura 4 mostra i fattori attivi della dieta antinfiammatoria, principalmente vegetariana e ricca di funghi, legumi, pesce, molluschi, crostacei, pasta integrale, cioccolato fondente, yogurt magro, frutta, funghi, legumi, pesce, molluschi, crostacei, pasta integrale, cioccolato fondente, fibre magre. Questa dieta, che è intesa come essere povera di pane e caseinati, si basa sull’assunzione di verdura, yogurt, spezie, spezie, olio extravergine di oliva, olio di caffè, caffè e thé.
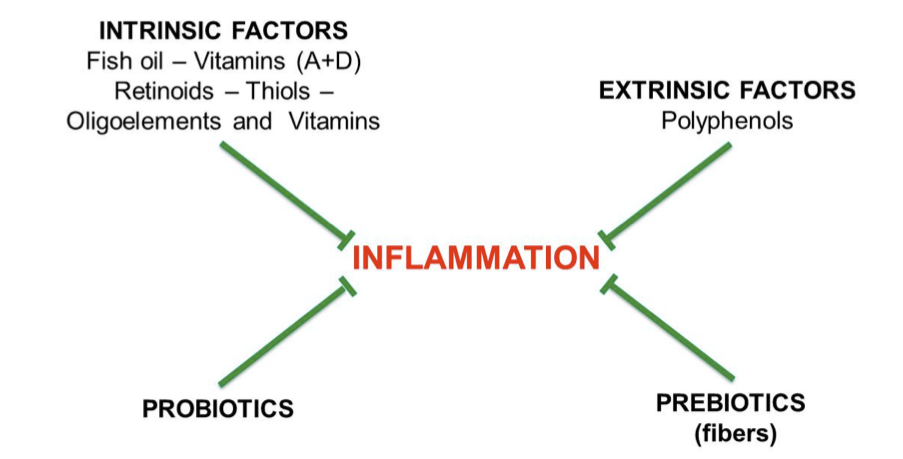
Figura 4. Fattori dietetici antinfiammatori. I fattori intrinseci sono quelli che svolgono un ruolo nel nostro metabolismo. Includono: omega-3 (PUFA n-3), presenti nell’olio di pesce; vitamine A e D, B12, PP, E e C; oligoelementi come magnesio, zinco e selenio; vitamine A e D, B12, PP, E e C; oligoelementi come magnesio, zinco e selenio; presenti nel metabolismo tiolico. acidi come: acido alfa-lipoico omega-3 (ALA), N-acetil cisteina polinsaturi a catena lunga e glutatione. acidi grassi I fattori estrinseci sono oligoelementi come magnesio, zinco e selenio; l’olio di pesce; polifenoli, vitamine A e fitochimici D, B12, PP, E e C presenti nelle verdure: hanno proprietà antinfiammatorie e regolano positivamente il catabolismo, ma sono riconosciuti dal nostro metabolismo come molecole “estranee”. Tuttavia, come mostrato di seguito, rappresentano una fonte di cibo per il microbiota intestinale. Prebiotici e probiotici sono citati qui per la loro azione antinfiammatoria, ma i loro effetti si esercitano principalmente attraverso il microbiota intestinale.
7. Cos’è il cibo e perché deve essere digerito
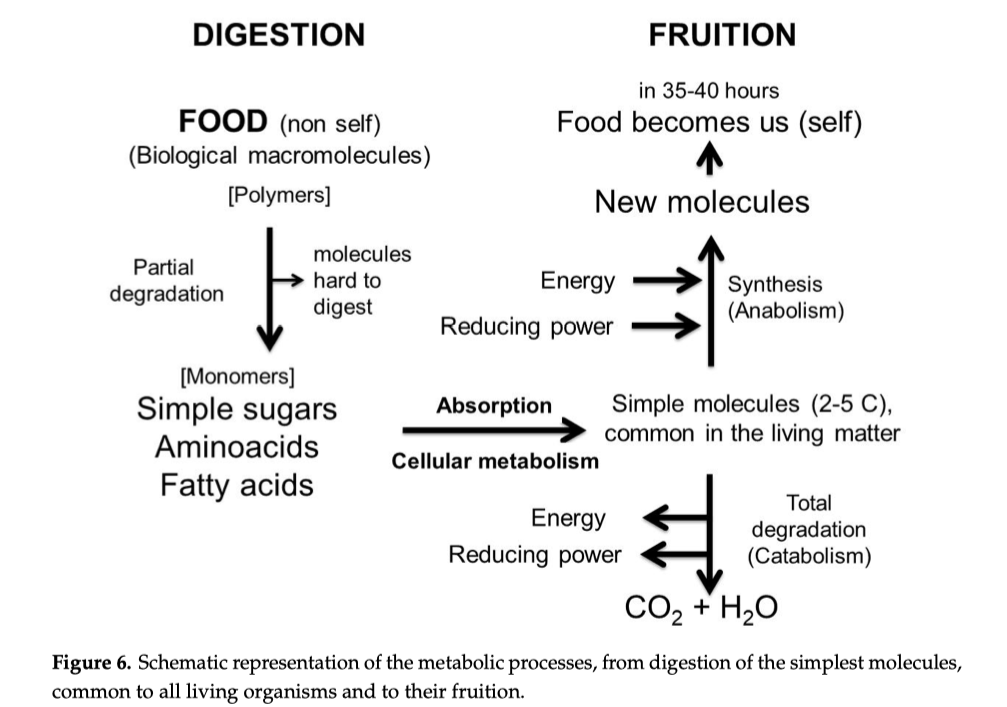
Essendo di origine diversa dalla nostra, tessuti, cellule e proteine del cibo non possono essere utilizzati così come sono, devono essere degradati in molecole semplici dall’apparato digerente nel tratto gastrointestinale (il recipiente di reazione) e poi assorbiti. Ecco perché il cibo deve essere digerito prima di essere assorbito: è non-self prima della digestione e diventa self quando la digestione è completa. Solo le molecole completamente digerite ci sono congeniali, sono riconosciute come self e possono entrare nel nostro metabolismo dopo il loro asorbimento.
11.3 Vitamine
È stato recentemente dimostrato che la vitamina A migliora l’integrità della barriera intestinale, anche in presenza di infiammazione intestinale e livelli elevati di LPS. Sembra contrastare l’azione dell’LPS e aumentare l’espressione delle proteine delle giunzioni strette [78].
Tuttavia, la vitamina A non è sufficiente. Come riportato nella nostra precedente revisione [25], la vitamina A e la vitamina D hanno effetti antinfiammatori sinergici e dovrebbero essere somministrate insieme. Ciò non sorprende, poiché entrambe sono liposolubili e spesso presenti insieme nello stesso alimento. I loro recettori nucleari cooperano se entrambe le vitamine si legano a loro. Le funzioni condivise della vitamina A e della vitamina D includono il potenziamento delle proteine delle giunzioni strette, la soppressione di IFN-γ e IL-17 e l'induzione delle cellule T regolatorie (Treg) [79]. Infine, le vitamine A e D sono efficaci contro l'infiammazione cronica e favoriscono la stabilità della barriera intestinale. La loro azione sul microbiota non è diretta poiché i loro recettori nucleari sono espressi solo dall'ospite, non dal microbiota. La carenza di vitamina D porta alla rottura della barriera intestinale, alla disbiosi intestinale e all'infiammazione intestinale [80].
In sintesi vitamina A e D:
-
rafforzano le giunzioni strette
-
sopprimono IFN-γ e IL-17
-
inducono Treg
-
contrastano infiammazione cronica
La carenza di vitamina D è associata a:
-
disbiosi
-
aumento permeabilità
-
infiammazione intestinale
12. Dalla disbiosi intestinale alla rottura della barriera emato-encefalica e all’infiammazione cerebrale
Il microbiota intestinale e le molecole di cibo non digerito cooperano nell'attacco alla barriera emato-encefalica. A prima vista, può sembrare strano che una condizione disbiotica intestinale possa portare al danno della barriera emato-encefalica (BEE). Tuttavia, nel corso di una disbiosi intestinale protratta, il normale dialogo tra intestino e SNC (central nervous system) [86–88] viene in qualche modo interrotto dalle molecole che fuoriescono dal lume intestinale e si riversano nel flusso sanguigno, innescando un'infiammazione sistemica cronica. La formazione di anticorpi contro le molecole di cibo non digerito, che assomigliano ad alcune proteine cerebrali, può indirizzare i processi pro-infiammatori verso la BEE e causarne la rottura. Infatti, ciò che è stato in grado di rendere la barriera intestinale più permeabile può avere lo stesso effetto anche sulla BEE. La sede della barriera ematoencefalica (BEE) sono i capillari cerebrali. Le loro cellule endoteliali sono fuse tra loro dalle giunzioni strette tra le proteie claudine, occludina e zona occludente, come nella barriera intestinale. Pertanto, il passaggio di molecole e cellule tra il sangue e il cervello è assolutamente limitato. In condizioni normali, solo le molecole idrofobiche e quelle dotate di un sistema di trasporto specifico (ad esempio, D-glucosio e amminoacidi essenziali) possono attraversare la BEE. Una differenza importante tra la BEE e la barriera intestinale è che la BEE è circondata dagli pseudopodi (le proiezioni della membrana) degli astrociti. La persistenza di molecole e cellule derivate dall'intestino in prossimità della barriera emato-encefalica può causarne la degradazione [89].
In sintesi la disbiosi intestinale cronica può:
-
generare infiammazione sistemica
-
produrre anticorpi contro antigeni alimentari
-
favorire mimetismo molecolare
-
contribuire alla rottura della barriera emato-encefalica
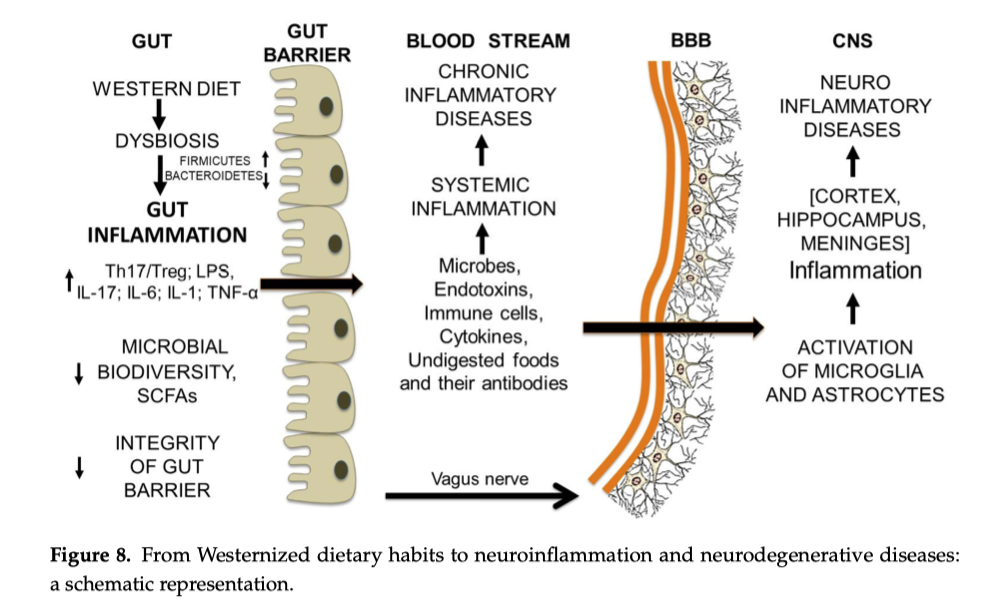
La BBB è costituita da cellule endoteliali unite da tight junctions e supportate dagli astrociti.
13. Conclusioni
Il percorso che porta alla malattia coinvolge il microbiota e frammenti di cibo non digerito, oltre a richiedere l’interruzione della barriera intestinale e della barriera emato-encefalica. La sequenza suggerita degli eventi è la seguente: (1) diete pro-infiammatorie protratte nel tempo, modificano la composizione del microbiota intestinale e inducono disbiosi del microbiota intestinale; (2) il sistema immunitario viene attivato e l’infiammazione intestinale aumenta, i livelli di cellule T e LPS aumentano; (3) la barriera intestinale diventa permeabile e il contenuto luminale (microbi, molecole di cibo non digerito, endotossine, cellule T e citochine) fuoriesce e innesca un’infiammazione sistemica cronica; (4) la risposta immunitaria contro frammenti di cibo non digerito che assomigliano a molecole cerebrali indirizza le molecole pro-infiammatorie alla BBB e ne provoca la rottura; (5) il passaggio attraverso la BBB di cellule e molecole pro-infiammatorie attivate provoca l’attivazione di cellule microgliali e astrociti (Le cellule microgliali sono le cellule immunitarie del cervello, mentre gli astrociti supportano i neuroni e contribuiscono alla barriera emato-encefalica ) e l’insorgenza di processi infiammatori in diverse aree cerebrali.
Nel presente articolo evidenziamo il possibile ruolo dei frammenti di cibo non digerito come agenti pro-infiammatori e l’importanza dell’integrità delle due barriere, intestinale e della barriera emato-encefalica (BEE), per la salute umana. Se la barriera intestinale diventa permeabile, frammenti di cibo non digerito fuoriescono anche dallo spazio luminale (intestino) insieme a batteri, endotossine, molecole immunocompetenti e cellule. Tutto questo materiale, che si supponeva rimanesse segregato nell’intestino, è ora in circolazione. Di solito ci preoccupiamo della disseminazione batterica, ma la disseminazione di cibo non digerito che attraversa la barriera intestinale e entra nel flusso sanguigno non deve essere trascurata.
Nell’intestino, i peptidi non completamente digeriti, sebbene ancora diversi da noi (non-self), erano sulla buona strada per diventare simili a noi (self), quindi la loro probabilità di mimetismo molecolare con i nostri peptidi potrebbe aumentare dopo una digestione parziale. Nel corso della disbiosi intestinale e dell’infiammazione intestinale, i linfociti T vengono attivati. Con l’attivazione dei linfociti T, i linfociti B vengono attivati per produrre anticorpi. Questi anticorpi contro gli antigeni alimentari possono riconoscere gli autoantigeni e innescare una risposta autoimmune. Ad esempio, è stato suggerito che gli anticorpi contro le proteine del grano e del latte nei donatori di sangue possano contribuire alle attività neuroimmuni [39].
Pertanto, i peptidi ( di aminoacidi) non digeriti e i loro anticorpi possono rafforzare le attività infiammatorie e autoimmuni e possono indirizzarle verso uno dei diversi organi, ma è necessaria la cooperazione con il microbiota.
Sequenza proposta:
-
Dieta pro-infiammatoria → disbiosi
-
Attivazione immunitaria → infiammazione intestinale
-
Permeabilità intestinale → infiammazione sistemica
-
Risposta autoimmune contro antigeni alimentari
-
Rottura BBB → neuroinfiammazione
Il cibo non digerito, insieme al microbiota disbiotico, può contribuire a processi infiammatori sistemici e autoimmuni.
Approfondimenti
A – Integrità barriera intestinale e malattie
Cause della compromissione della barriera intestinale:
-
Disbiosi:
Uno sbilanciamento del microbiota intestinale, con un aumento di batteri patogeni e una diminuzione di quelli benefici, può danneggiare la barriera.
-
Infiammazione:
Stati infiammatori cronici, dovuti a vari fattori come cattiva digestione, stress o infezioni, possono compromettere l’integrità della barriera.
-
Infezioni:
Infezioni intestinali da batteri, virus o parassiti possono danneggiare direttamente le cellule epiteliali.
-
Malattie autoimmuni:
In malattie come la celiachia e il morbo di Crohn, il sistema immunitario attacca erroneamente le cellule intestinali, causando infiammazione cronica e danni alla barriera.
-
Altre cause:
Fattori ambientali, come l’esposizione a tossine e inquinanti alimentari, e abitudini di vita poco sane possono contribuire alla compromissione della barriera.
Malattie associate alla compromissione della barriera intestinale:
-
Malattie gastrointestinali:
Sindrome dell’intestino irritabile, malattie infiammatorie intestinali (MORB, Colite ulcerosa), celiachia, sindrome dell’intestino gocciolante.
-
Malattie autoimmuni:
Artrite reumatoide, sclerosi multipla, diabete di tipo 1, lupus.
-
Disturbi metabolici:
-
Obesità, diabete di tipo 2, insulino-resistenza, steatosi epatica non alcolica.
-
Malattie neuroinfiammatorie:
Disturbi depressivi, ansia, disturbo dello spettro autistico, sindrome da stanchezza cronica.
-
Altre malattie:
Asma bronchiale, rinosinusite cronica, rinite allergica, dermatite atopica, esofagite eosinofila, tumori.
B – Linfociti T e B
I linfociti T (o cellule T) e i linfociti B (o cellule B) sono due tipi di globuli bianchi che svolgono un ruolo cruciale nel sistema immunitario. I linfociti T sono responsabili dell’immunità cellulo-mediata, mentre i linfociti B sono coinvolti nell’immunità anticorpo-mediata.
L’immunità cellulo-mediata (o immunità cellulare) è una risposta del sistema immunitario che coinvolge i linfociti T, in particolare i linfociti T citotossici e i linfociti T helper, per eliminare cellule infette o anomale. Questo tipo di immunità è fondamentale per difendere l’organismo dalle infezioni intracellulari, come quelle virali, e dalle cellule tumorali.
La risposta anticorpo-mediata (linfociti B ) è un secondo esempio di risposta immunitaria specifica, cioè di una difesa che preveda il riconoscimento specifico di un patogeno che abbia superato le difese dell’immunità innata.
Un antigene è una molecola (spesso una proteina) in grado di essere riconosciuta dal sistema immunitario come estranea o potenzialmente pericolosa provocando una risposta immunitaria specifica. Questa risposta si traduce nella produzione di anticorpi che riconoscano e si leghino all’antigene, neutralizzandolo.
Si definisce invece immunogena una sostanza in grado di stimolare il sistema immunitario a tentare di produrre anticorpi contro di essa.
In pratica, “immunogenica” descrive una caratteristica, mentre “immunogena” indica una sostanza che possiede tale caratteristica.
Note
1 – Le note riassuntive derivano dalla traduzione di alcuni passagi della ricerca:
Undigested Food and Gut Microbiota May Cooperate in the Pathogenesis of Neuroinflammatory Diseases: A Matter of Barriers and a Proposal on the Origin of Organ Specificity. Paolo riccio e Rocco Rossano.
Department of Sciences, University of Basilicata, 85100 Potenza, Italy; paoloxriccio@gmail.com Correspondence: rocco.rossano@unibas.it. Received: 1 October 2019; Accepted: 8 November 2019; Published: 9 November 2019. Nutrients 2019, 11, 2714; doi:10.3390/nu11112714.
2 – La numerazione dei capitoli fa riferimento agli analoghi capitoli della ricerca di cui al punto 1.
3 – I numeri in parentesi quadra si riferiscono alle referenze citate nella ricerca di cui al punto 1.
Nota finale conclusiva
Le evidenze scientifiche attuali indicano che l’intestino non è soltanto un organo digestivo, ma un centro regolatore cruciale dell’equilibrio immunitario, metabolico e neurobiologico. Attraverso il microbiota e la barriera mucosale, esso dialoga costantemente con il sistema immunitario e con il sistema nervoso centrale, configurando il cosiddetto asse intestino–sistema immunitario–cervello.
Quando questo asse è in equilibrio, contribuisce alla regolazione della tolleranza immunitaria e al mantenimento dell’omeostasi infiammatoria. Quando invece si altera — per disbiosi, aumento della permeabilità intestinale o stimoli alimentari pro-infiammatori — può instaurarsi uno stato di attivazione immunitaria cronica di basso grado che, nel tempo, si riflette non solo sul metabolismo ma anche sulla funzione neurologica.
In questo contesto, l’alimentazione assume un ruolo centrale. Non è un fattore neutro. Può sostenere la resilienza dell’asse intestino–immunità–cervello oppure contribuire alla sua destabilizzazione, soprattutto nei soggetti con predisposizioni genetiche, fragilità metaboliche, patologie infiammatorie o condizioni di salute già compromesse.
In un soggetto realmente “sano”, il sistema immunitario e gli organi deputati alla regolazione dell’omeostasi sono fisiologicamente in grado di mantenere lo stato di salute e di difendere l’organismo dagli agenti esterni, inclusi quelli alimentari. Questo equilibrio dipende dalla capacità dell’organismo di modulare le risposte infiammatorie, preservare l’integrità della barriera intestinale e mantenere una corretta comunicazione tra intestino, sistema immunitario e sistema nervoso.
Tuttavia, nei soggetti con predisposizioni genetiche, vulnerabilità immunologiche o condizioni cliniche già presenti — anche se non sempre clinicamente manifeste — un criterio di prudenza nutrizionale non rappresenta un eccesso di cautela, bensì un atto di responsabilità preventiva. In questi casi, l’alimentazione può contribuire a modulare positivamente o negativamente l’equilibrio infiammatorio e immunitario.
La qualità dell’alimentazione quotidiana, infatti, non influisce esclusivamente sull’intestino: incide sul tono immunitario, sul livello di infiammazione cronica di basso grado e, indirettamente, anche sulla salute cerebrale attraverso i complessi meccanismi dell’asse intestino–cervello. Prendersi cura dell’intestino significa, in larga misura, prendersi cura dell’intero organismo. È necessario, infine, precisare che per “soggetto sano” non si intende semplicemente un individuo privo di malattie clinicamente manifeste, ma una persona senza patologie in atto e senza uno stato di infiammazione cronica di basso grado. Questa distinzione è fondamentale, poiché nella pratica clinica il termine “sano” viene spesso utilizzato in senso limitato, coincidente con la sola assenza di diagnosi formali.
Bibliografia
Drago S., et al. (2006)
Gliadin, zonulin and gut permeability: Effects on celiac and non-celiac intestinal mucosa Gut.
– Mostra che la gliadina può attivare la via zonulina e aumentare la permeabilità, ma principalmente nel contesto della mucosa intestinale che già reagisce. (PubMed)
Fasano A. (2012) Intestinal Permeability and its Regulation by Zonulin. Physiological Reviews.
– Descrive il coinvolgimento della via zonulina nella regolazione delle tight junctions, ma sottolinea che esistono altri meccanismi modulanti la permeabilità. (PMC)
Manza F., et al. (2025). Non-Celiac Gluten/Wheat Sensitivity — State of the Art .
Nutrients. DOI: 10.3390/nu17020220
– Review recente che conferma come la zonulina possa essere correlata a permeabilità ma evidenzia che gli effetti di glutine variano tra individui e condizioni. (MDPI)
Stojanov S., et al. (2020)
The Influence of Probiotics on the Firmicutes/Bacteroidetes Ratio and Obesity
Microorganisms.
– Anche se non esclusivamente dedicato ai dolcificanti, sottolinea che il microbiota è molto variabile e che i risultati dipendono da molti fattori. (MDPI)
Harach T., et al. (2015)
Reduction of Alzheimer’s disease beta-amyloid pathology in the absence of gut microbiota
PNAS (preprint / lavoro citato).
– Studio animale che indica come l’assenza di microbiota possa ridurre patologia Alzheimer-like, ma non è tradotto direttamente in evidenza causale umana. (arXiv)
Veres-Székely A., et al. (2023)
Zonulin as a Potential Therapeutic Target in Microbiota-Gut-Brain Axis Disorders
International Journal of Molecular Sciences.
– Riporta dati sperimentali su modello murino dove alti livelli di zonulina sono associati a permeabilità intestinale e a compromissione BBB, ma evidenzia la necessità di ulteriori conferme. (MDPI)
Sapone A., et al. (2006)
Differential mucosal immune-responses to gliadin along the small intestine in celiac disease — Include dati su tight junctions e funzioni di barrier.
Riassunto dei riferimenti principali
|
Tema |
Autore e anno |
Titolo |
Fonte / DOI |
|---|---|---|---|
|
Zonulina problematic ELISA |
Ajamian et al., 2019 |
Serum zonulin… |
10.1371/journal.pone.0210728 |
|
Zonulina come biomarker criticato |
Massier et al., 2020 |
How shortcomings… |
Gut 70(9):1801–10 |
|
Gliadina e zonulina |
Drago et al., 2006 |
Gliadin, zonulin and gut permeability |
PubMed |
|
Regulation of tight junctions |
Fasano, 2012 |
Intestinal Permeability and its Regulation by Zonulin |
PubMed |
|
F/B ratio review |
Magne et al., 2020 |
The Firmicutes/Bacteroidetes Ratio… |
Microorganisms 8(11):1715 |
|
Zonulina e microbiota-brain |
Veres-Székely et al., 2023 |
Zonulin as a Therapeutic Target… |
Int J Mol Sci |
Back

