(L’infiammazione cronica di basso grado non è una malattia in senso stretto, ma uno stato biologico persistente che favorisce lo sviluppo di numerose patologie croniche. Il presente documento propone un approccio integrato orientato alla sua modulazione attraverso lo stile di vita.)
Inoltre:
In assenza di soluzioni univoche e definitive, la strategia più razionale per ridurre l’infiammazione cronica di basso grado consiste nell’adottare un modello di vita che minimizzi l’esposizione ai fattori potenzialmente pro-infiammatori* e favorisca quelli protettivi.
L’importanza dell’infiammazione cronica di basso grado.
Sebbene l’aumento intermittente dell’infiammazione sia fondamentale per la sopravvivenza durante lesioni fisiche e infezioni, recenti ricerche hanno rivelato che alcuni fattori sociali, ambientali e legati allo stile di vita possono favorire l’infiammazione cronica sistemica, in particolare l’infiammazione cronica di basso grado (ICBG), che, a sua volta, può portare a diverse patologie che, nel loro insieme, rappresentano le principali cause di disabilità e mortalità in tutto il mondo, come malattie cardiovascolari, cancro, diabete mellito, malattia renale cronica, steatosi epatica non alcolica e malattie autoimmuni e neurodegenerative. (vedi articolo: https://glutenlight.eu/2025/08/21/infiammazione-cronica-basso-grado/
Questo tipo di infiammazione ha molteplici fattori scatenanti:
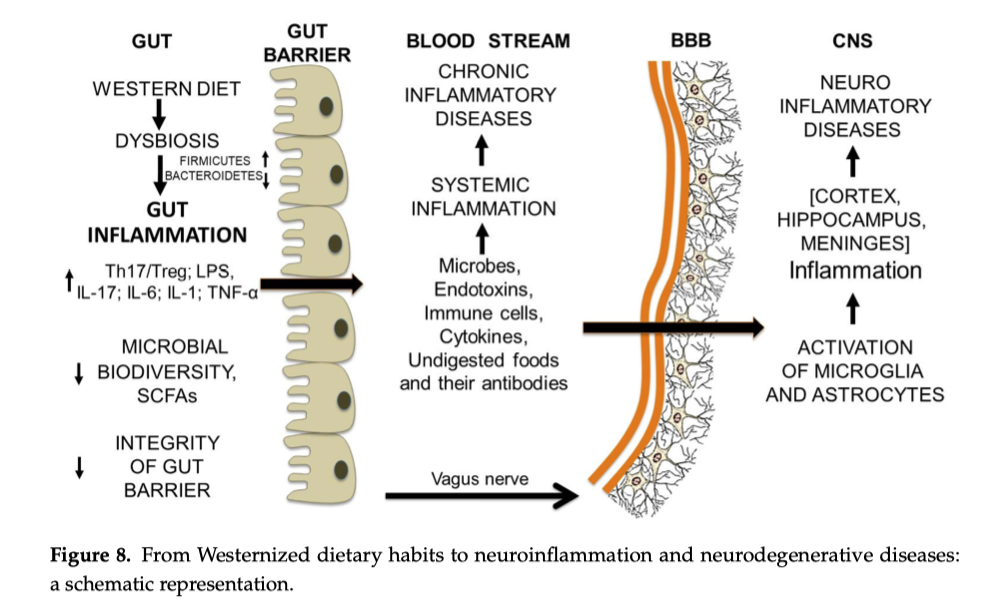
Disbiosi intestinale:
Alterazione della flora batterica intestinale, che può essere causata da dieta squilibrata, uso eccessivo di antibiotici o altre sostanze tossiche.
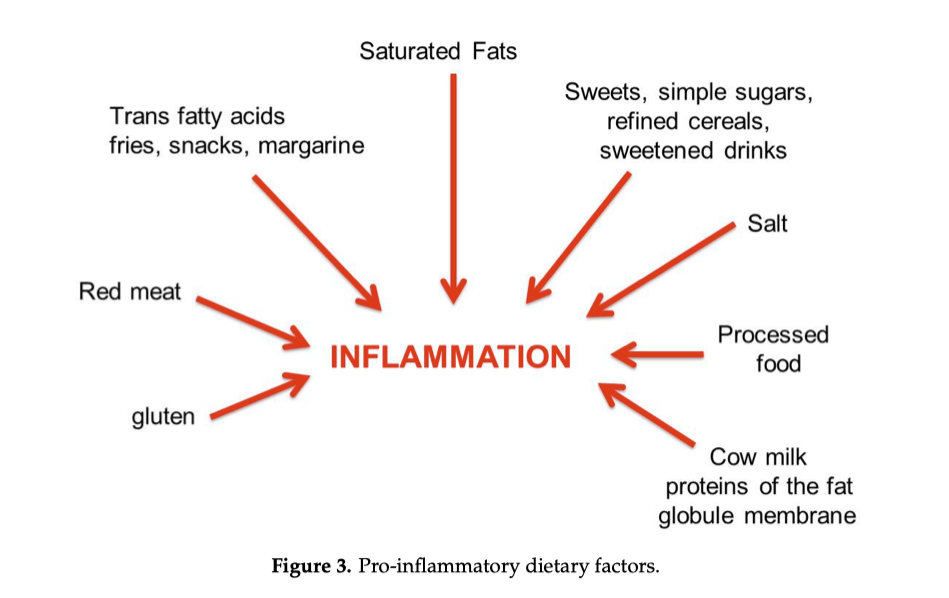
Dieta scorretta:
Consumo eccessivo di cibi processati, ricchi di zuccheri raffinati e grassi saturi, che possono favorire l’infiammazione.
Stress:
Lo stress cronico può influenzare negativamente il sistema immunitario e aumentare la suscettibilità all’infiammazione.
Inquinamento ambientale e tossine:
Esposizione a sostanze chimiche presenti nell’ambiente o nei cibi può contribuire allo stress ossidativo e all’infiammazione.
Fumo e alcol:
Questi fattori possono aggravare lo stress ossidativo e danneggiare le cellule, favorendo l’infiammazione. (vedi articolo: Stess ossidativo)
Tra i fattori scatenanti non compare l’uso di droghe perché considerate sempre e comunque da evitare.
L’Approccio integrato deve necessariamente interessare l’individuo in tutti gli aspetti della sua vita. Questo è il punto centrale: va “costruito” un modello di vita. E questo modello deve essere personalizzato.
Altra considerazione riguarda lo stato di salute generale dell’individuo che deve prioritariamente mantenersi “sano”, cioè senza malattie, traumi, ferite, ecc., che attivano l’infiammazione acuta.
È importante sottolineare che, in presenza di infiammazione acuta, i marker biologici utilizzati per valutare l’infiammazione cronica di basso grado risultano elevati, rendendo difficile distinguere i due fenomeni e potendo mascherare eventuali miglioramenti dell’ICBG.
Fatte queste precisazioni possiamo iniziare l’ Approccio integrato
1 – Gestione dello stress.
È un fattore molto importante considerate le emergenti evidenze scientifiche riguardanti l’asse intestino-cervello, un sistema di comunicazione bidirezionale attraverso il quale stress psicologico, emozioni e stati mentali influenzano la motilità intestinale, la permeabilità della barriera e la composizione del microbiota, e viceversa. Alterazioni di questo asse possono favorire infiammazione, disturbi digestivi e squilibri metabolici.
Lo stress deve essere gestito o in autonomia con le tecniche esistenti o se non possibile con l’aiuto di uno psicologo.
2 – Inquinamento ambientale (aria, acqua, ecc): va da se che più riusciamo ed evitarlo meglio è. Questo fattore è rilevante per lo stess ossidativo.
3 – Alimentazione: qui possiamo fare molto
Punto importante:
L’alimentazione va strettamente correlata con l’età, l’attività svolta, le abitudini alimentari, lo stato di salute generale.
Cibi da evitare
-
Cibi industriali: contengono additivi che, se assunti singolarmente una volta ogni tanto non creano problemi ma, se assommati tra loro, possono avere un’azione pro-infiammatoria più o meno marcata in relazione allo stato di salute del soggetto [A].
-
Bevande industriali: generalmente contengono molti zuccheri/edulcoranti/additivi.
-
Molti prodotti senza glutine (soprattutto industriali) sono altamente processati e contengono additivi (spesso molti) che, se assunti singolarmente una volta ogni tanto non creano problemi ma, se assommati tra loro, possono avere un’azione pro-infiammatoria in relazione allo stato di salute del soggetto.
Cibi da assumere con moderazione
-
Vino/birra: con moderazione
-
Alcolici: in casi saltuari (superalcolici: NO)
-
Caffè: con moderazione
-
Insaccati: con molta moderazione
-
Dolci: con moderazione. Se problemi con gli zuccheri (per peso o per glicemia) vanno assunti nelle dosi opportune per non avere problemi.
-
Formaggi: con molta moderazione e nella misura compatibile con il soggetto (se intolleranti al lattosio/proteina caseina)
-
Spezie: con moderazione
-
Grassi: meno trans (idrogenati) e, in misura minore, quelli saturi in eccesso e più olio extravergine d’oliva (acido oleico)
- Zuccheri raffinati: meno se ne assumono meglio è. Inoltre va ricordato come picchi frequenti di glucosio e insulina stimolino la produzione di citochine pro-infiammatorie.
-
Glutine: con moderazione. Se possibile pasta integrale/semintegrale; pane: se possibile integrale di grano duro/farro. Il grano tenero contiene una componente del glutine molto difficile da digerire (33mer). Considerato il legame esistente tra la forza del glutine e sua digeribilità vanno possibilmente privilegiati prodotti realizzati con grani che hanno un glutine meno tenace. Tra i “grani antichi” si possono trovare parecchi con questa caratteristica (in realtà anche tra grani moderni ci sono cultivar con glutine meno tenace: vengono usati per realizzare dolci ma non pane): andrebbero privilegiati. Chi è intollerante al glutine ma non celiaco considerato che questa intolleranza è “dose dipendente” può, con l’aiuto di un medico, cercare quale la soglia (quantità) che non da problemi. Grani con glutine meno tenace favoriscono la possibilità di consumare prodotti con essi realizzati. Approfondimento: Differenza tra grani antichi e moderni (Pubblicato a parte)
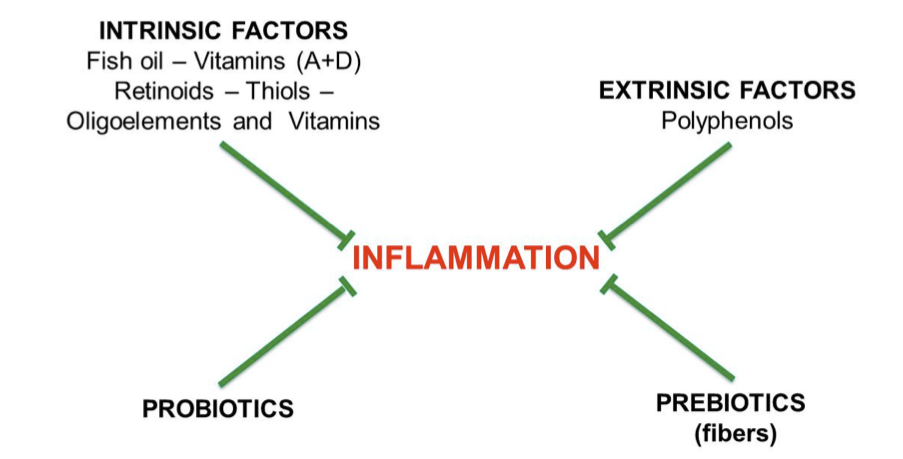
Cibi da assumere in abbondanza:
-
Fibre (compatibilmente con eventuali problematiche a livello intestinale): 3/4 volte al giorno.
- Frutta (compatibilmente con eventuali problemi con gli zuccheri: glicemia e/o peso)
- The verde ottimo alleato. Il tè verde è considerato un potente alleato contro l’infiammazione cronica grazie alla sua ricchissima composizione di composti bioattivi che agiscono su più fronti dell’organismo [D].
A parte va ricordato l’essenziale contributo dell’acqua per mantenere una efficiente idratazione. Il sistema linfatico è una sorta di rete di drenaggio dell’infiammazione cronica.
Ma funziona bene solo se c’è abbastanza acqua. Se bevi poco: la linfa ristagna, le tossine rimangono nei tessuti, l’infiammazione “di sottofondo” aumenta vedi: Il ruolo dell’acqua nella riduzione dell’infiammazione di basso grado
4– Comportamenti nell’alimentazione
L’alimentazione poggia su due pilastri principali: quantità e qualità.
La quantità di cibo da assumere dovrebbe essere quella necessaria per le funzioni fisiologiche più quella necessaria per le attività svolte. Questo semplice principio ci aiuterebbe molto a mantenere un peso corretto e salutare. Proposito non facile per due semplici ragioni:
la prima è la “gola”, la seconda è che il meccanismo del “pieno/sazio” è posposto al pieno effettivo, cioè la sensazione di essere sazi non coincide con il riempimento reale dello stomaco, ma arriva dopo. Già 50 anni fa il medico di famiglia suggeriva di alzarsi da tavola con un leggero desiderio di altro cibo. La qualità: va da sé che più i cibi sono genuini e “puliti” (cioè privi di sostanze tossiche), meglio è.
Quanto segue deve inoltre considerarsi uno schema generale, perché, per quanto già detto, va “disegnato intorno al singolo individuo”.
A – Evitare il più possibile di assumere troppo cibo in un unico pasto
Lo stomaco dovrebbe essere messo in grado di lavorare (digerire) al meglio. È spesso preferibile mangiare più volte piuttosto che fare un unico pasto molto abbondante. Ottimo sarebbe: finire di mangiare e “non sentire lo stomaco” con la conseguenza di non avere “appannamenti” post prandiali. Approfondimento: Perche pasti più piccoli e distribuiti funzionano meglio. (Pubblicato a parte)
Il cibo non completamente digerito, nelle persone sane*, viene successivamente elaborato nell’intestino e poi espulso. Tuttavia, se il sistema gastrointestinale è compromesso o in stato di alterazione, il passaggio di substrati non adeguatamente digeriti all’intestino può favorire fermentazioni batteriche e risultare pro-infiammatorio. (https://glutenlight.eu/2025/06/12/cibo-non-digerito-e-infiammazione-intestinale/)
Non solo lo stomaco, ma anche e soprattutto l’intestino deve poter lavorare al meglio e continuare a digerire il cibo in modo da renderlo assimilabile. [B] [C]
*Qui il punto critico è: esiste ancora l’individuo realmente sano?
B – Evitare di mescolare cibi troppo differenti
Lo stomaco lavora in ambiente acido, dove la pepsina digerisce le proteine (ulteriormente digerite nell’intestino dalla tripsina e da altri enzimi). Gli zuccheri iniziano la digestione in bocca (ptialina) e vengono poi digeriti soprattutto nell’intestino (amilasi pancreatica). Qui è necessario fare alcune precisazioni:
Carboidrati e proteine nello stomaco non creano generalmente problemi.
Un primo di pasta seguito da pesce, carne, formaggio e magari verdure, in quantità adatte alla propria capacità digestiva, non crea problemi.
Se il secondo è un cibo molto grasso, va considerato che la digestione gastrica rallenta e, in dipendenza della quantità, può rallentare lo svuotamento gastrico, con possibile passaggio all’intestino di cibo non completamente digerito.
Diversa è la situazione se inseriamo nel pasto una porzione di dolce.
Qui ci troviamo di fronte a una quantità significativa di zuccheri semplici, non di carboidrati complessi (la pasta, ad esempio, è composta principalmente da amido, e solo una parte viene trasformata in zuccheri già nella bocca; quindi nello stomaco arriva soprattutto amido).
Gli zuccheri non vengono digeriti nello stomaco se non in misura trascurabile:
“The stomach has a highly acidic environment that prevents fermentation there; the undigested sugars travel to the small intestine and large intestine, where they are fermented by the gut bacteria.”
Il dolce a fine pasto (inteso come porzione moderata) non dà problemi a una persona sana (che oggi è relativamente rara), ma rende la digestione meno facile per molte persone, non solo per i possibili effetti intestinali successivi, ma anche per la sensazione di pesantezza che può comparire.
Va precisato che non è un dogma: esistono persone che digeriscono praticamente tutto senza difficoltà — siamo tutti diversi.
L’età, inoltre, gioca un ruolo fondamentale. La persona anziana tende a stare meglio quanto più semplice è il pasto. Approfondimento: Zuccheri e proteine nella digestione dello stomaco (Pubblicato a parte)
Punto importante
In caso di patologie legate all’alimentazione è strettamente necessario l’intervento di uno specialista (dietologo o nutrizionista).
5 – Comportamenti specifici :
-
Fare attività fisica anche solo moderatamente.
-
Se in attività lavorativa evitare che questa porti a stress. Lo stress va comunque gestito altrimenti è causa di infiammazione cronica di basso grado
-
Se sovrappeso è necessario eliminarlo.
-
Se in periodo post attività lavorativa impegnarsi in attività che richiedano concentrazione e, se possibile, creatività. Realizzare progetti è altamente utile per mantenere in attività le funzioni cerebrali
6 – Accertamenti:
Con il proprio medico definire gli accertamenti generali di routine necessari per un buon monitoraggio della propria salute oltre ad accertamenti specifici per eventuali patologie.
Sintesi Finale:
Dobbiamo costruire un modello di stile di vita personalizzato per la riduzione dell’infiammazione cronica di basso grado.
In una persona sana, un pasto contenente proteine e zuccheri in quantità moderate non crea problemi. L’associazione diventa potenzialmente problematica quando gli zuccheri sono molto concentrati, soprattutto in forma liquida e in quantità elevate. In persone con apparato gastrointestinale sensibile o alterato, anche porzioni moderate (come un dolce a fine pasto) possono causare discomfort digestivo.
L’approccio integrato alla riduzione dell’infiammazione cronica di basso grado si fonda sulle evidenze scientifiche disponibili, riportate nella sezione bibliografia.
Poiché molte ricerche mostrano associazioni significative senza dimostrare un rapporto causale assoluto, viene adottato un principio di precauzione: ridurre o eliminare, ove possibile, i fattori potenzialmente dannosi, privilegiando scelte a basso rischio biologico.
Read More