Questo articolo fa parte di una serie di approfondimenti sul rapporto tra sistema nervoso, microbiota e sindrome dell’intestino irritabile.
-
Parte 1 – Asse cervello-intestino: come stress e ansia influenzano la salute dell’intestino
-
Parte 2 – Intestino e cervello: il dialogo che spiega il colon irritabile
-
Parte 3 – Fodmap, IBS, infiammazione di basso grado e intestino vulnerabile
1. Introduzione
La sindrome dell’intestino irritabile (Irritable Bowel Syndrome, IBS) è uno dei disturbi gastrointestinali funzionali più comuni, caratterizzato da dolore addominale ricorrente associato ad alterazioni dell’alvo in assenza di patologia organica evidente. La prevalenza nella popolazione generale è stimata tra il 10% e il 15%, con un impatto significativo sulla qualità della vita e sui costi sanitari [1].
Negli ultimi due decenni la dieta a basso contenuto di FODMAP (Fermentable Oligo-, Di-, Mono-saccharides And Polyols) si è affermata come uno degli interventi dietetici più efficaci per il controllo dei sintomi della IBS [2].
I FODMAP sono carboidrati a corta catena scarsamente assorbiti nel piccolo intestino e rapidamente fermentati dal microbiota colico. Questo processo può determinare un aumento del carico osmotico intraluminale e una maggiore produzione di gas, contribuendo alla distensione intestinale e alla comparsa di sintomi quali dolore addominale, gonfiore e alterazioni dell’alvo [3].
Tuttavia, è sempre più evidente che i FODMAP non rappresentano di per sé un fattore patologico universale. Molti individui sani tollerano quantità elevate di questi carboidrati senza sviluppare sintomi gastrointestinali significativi. Questo suggerisce che l’effetto sintomatologico dei FODMAP dipenda in larga parte dallo stato fisiologico dell’intestino e dalla presenza di condizioni predisponenti.
2. Il concetto di “intestino vulnerabile”
Negli ultimi anni diversi modelli patogenetici della IBS hanno introdotto il concetto di “vulnerable gut”, ovvero un intestino biologicamente predisposto a reagire in modo amplificato a stimoli fisiologici come la fermentazione intestinale o la distensione luminale [4].
In questo contesto i FODMAP agirebbero principalmente come trigger o amplificatori dei sintomi, piuttosto che come causa primaria della patologia.
Diversi fattori biologici possono contribuire alla vulnerabilità dell’intestino:
-
alterazioni della barriera intestinale
-
disbiosi del microbiota
-
ipersensibilità viscerale
-
alterazioni della motilità intestinale
-
attivazione immunitaria mucosale di basso grado.
Queste alterazioni possono abbassare la soglia di tolleranza agli stimoli intestinali, rendendo sintomatica una fermentazione che in condizioni fisiologiche sarebbe ben tollerata.
3. Infiammazione cronica di basso grado e IBS
Numerosi studi hanno dimostrato che una parte dei pazienti con IBS presenta segni di infiammazione mucosale di basso grado.
Questa condizione è caratterizzata da:
-
aumento di cellule immunitarie nella mucosa intestinale
-
maggiore attività dei mastociti
-
aumento della produzione di citochine pro-infiammatorie
-
alterazioni della permeabilità della barriera intestinale [5].
Questi cambiamenti immunologici sono stati osservati soprattutto nei pazienti con IBS post-infettiva, suggerendo che infezioni intestinali acute possano innescare un processo infiammatorio persistente che altera la funzione intestinale nel lungo termine [6].
L’infiammazione mucosale può contribuire allo sviluppo di ipersensibilità viscerale, una delle caratteristiche fisiopatologiche principali della IBS. In questa condizione stimoli normalmente innocui, come la distensione intestinale indotta dalla fermentazione dei FODMAP, possono generare dolore o disagio significativo.
Le evidenze disponibili indicano che l’attivazione immunitaria mucosale di basso grado è presente solo in un sottogruppo di pazienti con IBS, suggerendo che la sindrome possa comprendere diversi fenotipi fisiopatologici con meccanismi patogenetici parzialmente distinti.
4. Microbiota intestinale, fermentazione e sintomi
Il microbiota intestinale svolge un ruolo centrale nella digestione dei FODMAP.
La fermentazione batterica di questi carboidrati produce:
-
gas (idrogeno, metano e anidride carbonica)
-
acidi grassi a corta catena
-
metaboliti bioattivi.
In condizioni fisiologiche questi processi sono parte della normale digestione e contribuiscono alla salute metabolica dell’intestino.
Tuttavia, nei pazienti con IBS la fermentazione dei FODMAP può provocare una distensione intestinale eccessiva e attivare meccanismi neuro-immunitari che amplificano la percezione del dolore [7].
Diversi studi hanno inoltre evidenziato alterazioni nella composizione del microbiota nei pazienti con IBS, fenomeno noto come disbiosi, che potrebbe influenzare la risposta individuale alla dieta e alla fermentazione dei carboidrati [8].
5. FODMAP come amplificatori dei sintomi
Alla luce delle evidenze attuali, molti ricercatori considerano i FODMAP non tanto come fattori etiologici diretti della IBS, ma come amplificatori dei sintomi in individui predisposti.
In soggetti con una fisiologia intestinale integra, caratterizzata da:
-
barriera intestinale efficiente
-
microbiota stabile
-
bassa attivazione immunitaria mucosale
-
normale sensibilità viscerale,
la fermentazione dei FODMAP produce generalmente solo fenomeni fisiologici senza sintomi clinicamente rilevanti.
Al contrario, in individui con intestino vulnerabile, gli stessi stimoli possono determinare una cascata di eventi che culmina nella comparsa di dolore addominale, gonfiore e alterazioni dell’alvo.
6. IBS come continuum fisiopatologico
Le evidenze più recenti suggeriscono che la IBS possa rappresentare uno spettro di disfunzioni intestinali, piuttosto che una condizione patologica uniforme.
È possibile immaginare un continuum fisiopatologico:
-
intestino altamente resiliente → fermentazione fisiologica senza sintomi
-
intestino moderatamente sensibile → gonfiore occasionale
-
intestino vulnerabile → sintomi intermittenti compatibili con IBS
-
intestino ipersensibile → IBS clinicamente significativa.
In questo modello i FODMAP agiscono come fattori che possono amplificare i sintomi lungo questo spettro.
7. Mastociti intestinali e asse intestino-cervello
Negli ultimi anni crescente attenzione è stata rivolta al ruolo dei mastociti intestinali nella fisiopatologia della IBS.
I mastociti sono cellule del sistema immunitario presenti nella mucosa intestinale che svolgono un ruolo chiave nella risposta infiammatoria e nella comunicazione tra sistema immunitario e sistema nervoso enterico.
Numerosi studi hanno evidenziato che nei pazienti con IBS si osserva frequentemente:
-
aumento del numero di mastociti nella mucosa intestinale
-
maggiore attività di degranulazione mastocitaria
-
rilascio di mediatori infiammatori come istamina, triptasi e prostaglandine [9].
Questi mediatori possono agire direttamente sulle fibre nervose sensoriali presenti nella parete intestinale, aumentando la sensibilità viscerale e contribuendo alla percezione del dolore.
Il legame tra mastociti e sistema nervoso enterico rappresenta uno degli elementi centrali dell’asse intestino-cervello (gut–brain axis), un sistema di comunicazione bidirezionale tra intestino e sistema nervoso centrale.
L’attivazione mastocitaria può quindi amplificare la trasmissione dei segnali dolorosi dall’intestino al sistema nervoso centrale. In questo contesto, stimoli relativamente modesti come la distensione intestinale indotta dalla fermentazione dei FODMAP possono essere percepiti come dolorosi.
7.1 Stress, sistema nervoso autonomo e asse intestino-cervello
Oltre ai meccanismi neuro-immunologici locali descritti nel capitolo precedente, un ulteriore livello di regolazione della fisiopatologia della IBS riguarda il ruolo del sistema nervoso centrale, dello stress e del sistema nervoso autonomo.
L’intestino e il cervello comunicano attraverso una rete complessa definita asse intestino–cervello (gut–brain axis), che comprende:
-
sistema nervoso enterico
-
sistema nervoso autonomo (simpatico e parasimpatico)
-
asse ipotalamo–ipofisi–surrene (HPA)
-
segnali immunologici
-
metaboliti prodotti dal microbiota intestinale.
A differenza dei meccanismi descritti nel capitolo 7, che riguardano principalmente interazioni locali tra sistema immunitario mucosale e sistema nervoso enterico, il ruolo dello stress coinvolge una regolazione centrale, in cui il cervello modula direttamente la funzione intestinale.
Numerosi studi hanno dimostrato che lo stress psicologico e fisiologico può influenzare diverse funzioni gastrointestinali rilevanti nella IBS, tra cui:
-
motilità intestinale
-
secrezione intestinale
-
sensibilità viscerale
-
permeabilità della barriera intestinale
-
attività del sistema immunitario mucosale.
L’attivazione cronica dell’asse HPA e del sistema nervoso autonomo può determinare un aumento del rilascio di ormoni dello stress, come cortisolo e catecolamine, che a loro volta possono influenzare la funzione della mucosa intestinale e la composizione del microbiota.
Diversi modelli sperimentali suggeriscono inoltre che lo stress possa favorire:
-
aumento della permeabilità intestinale
-
attivazione dei mastociti intestinali
-
amplificazione della trasmissione dei segnali dolorosi viscerali.
In questo modo, i meccanismi centrali legati allo stress possono interagire con i meccanismi periferici descritti nel capitolo precedente. L’attivazione mastocitaria e la liberazione di mediatori infiammatori nella mucosa intestinale rappresentano infatti uno dei punti di connessione tra la regolazione centrale dello stress e la risposta immunitaria locale dell’intestino.
La IBS viene quindi sempre più interpretata come il risultato di interazioni bidirezionali tra cervello e intestino.
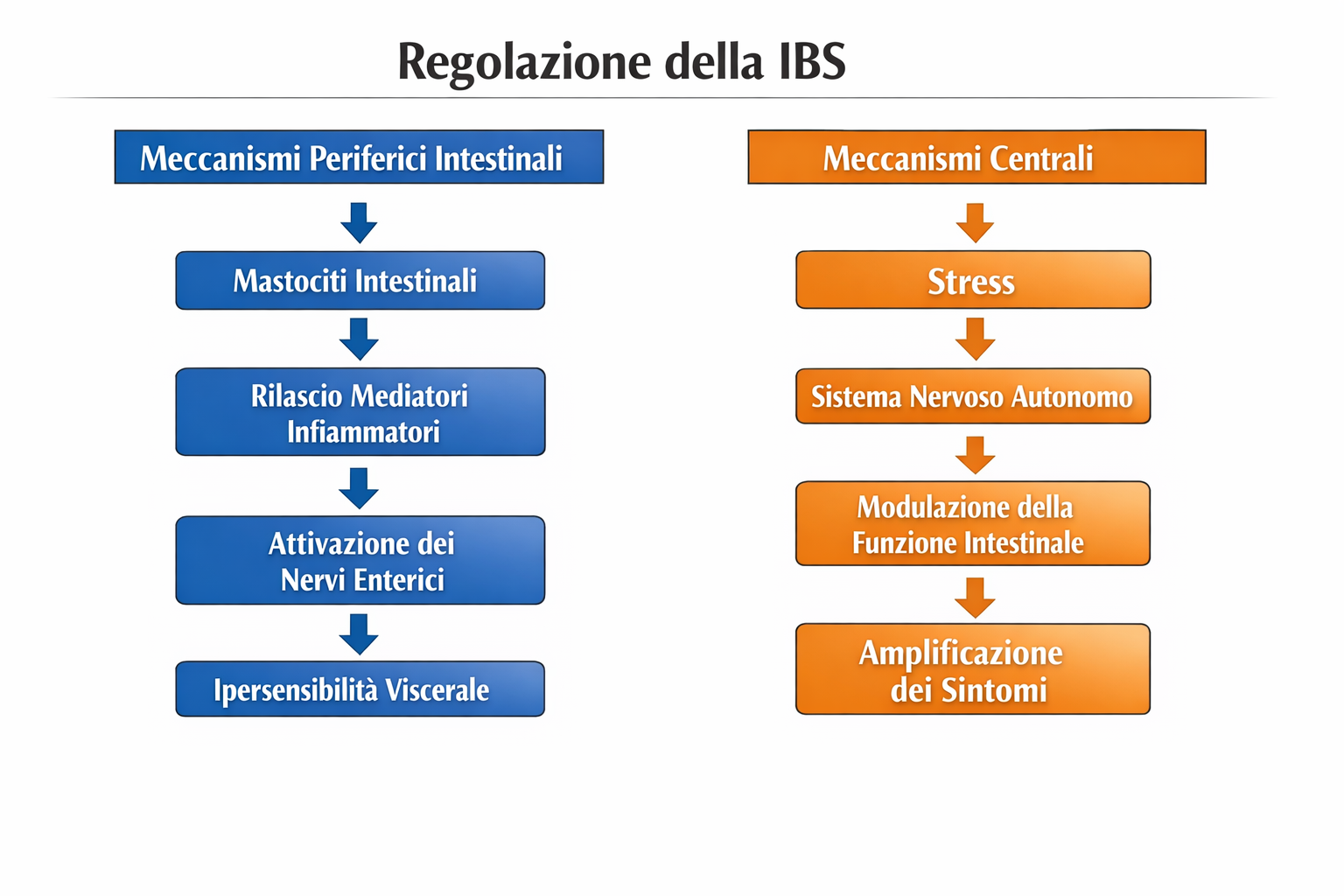
In questa prospettiva si possono distinguere due livelli complementari di regolazione:
Meccanismi periferici intestinali (capitolo 7)
mastociti intestinali → mediatori infiammatori → attivazione dei nervi enterici → ipersensibilità viscerale
Meccanismi centrali (presente sottocapitolo)
stress → sistema nervoso autonomo → modulazione della funzione intestinale → amplificazione dei sintomi.
L’integrazione di questi due livelli aiuta a spiegare perché fattori apparentemente diversi, come dieta, infezioni intestinali, disbiosi del microbiota o stress psicologico, possano contribuire allo sviluppo dei sintomi della IBS.
In questo modello fisiopatologico integrato, i FODMAP rappresentano uno stimolo fermentativo che può diventare sintomatogeno soprattutto quando l’intestino è già reso più sensibile da alterazioni della barriera epiteliale, attivazione immunitaria mucosale o modulazione centrale legata allo stress.