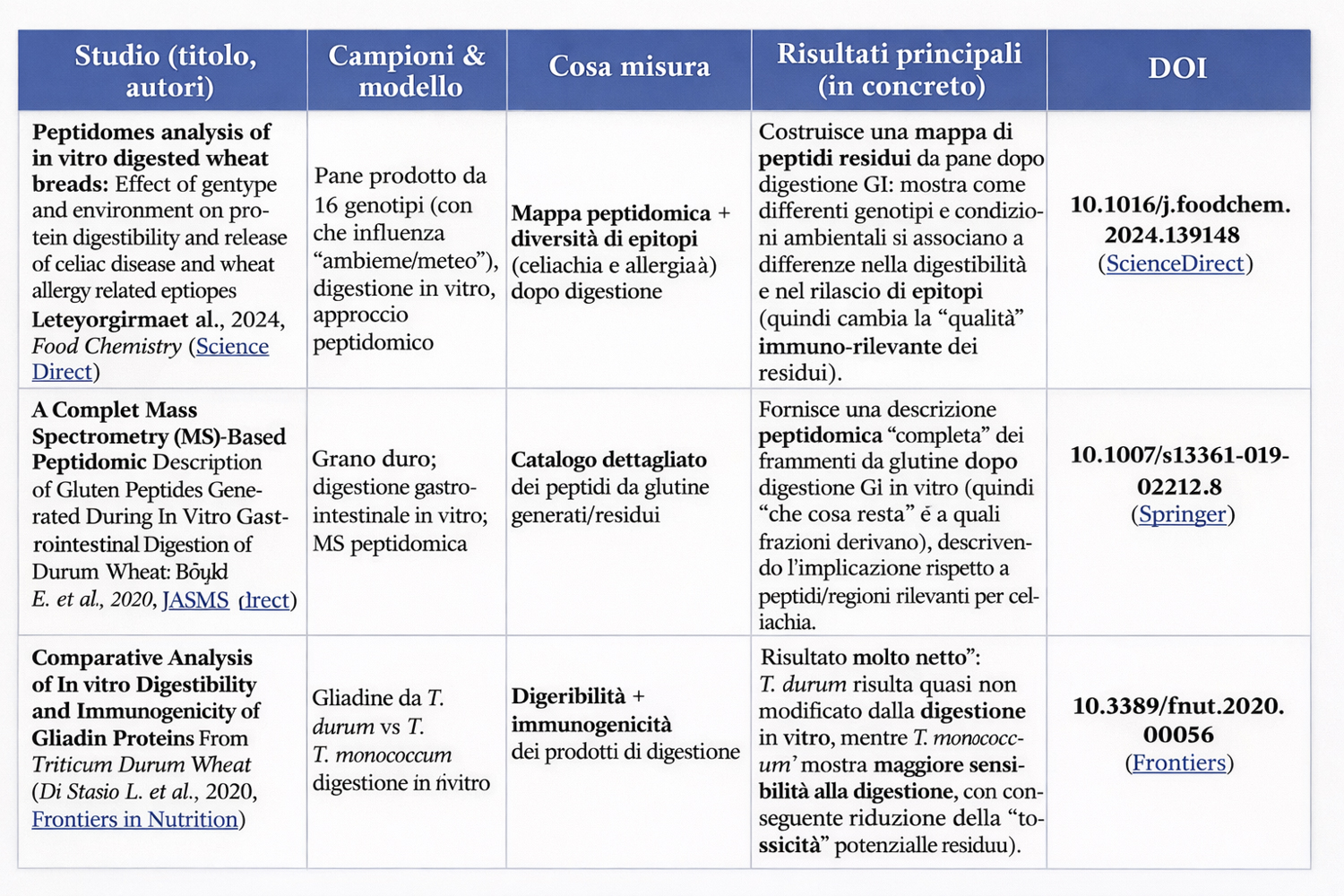
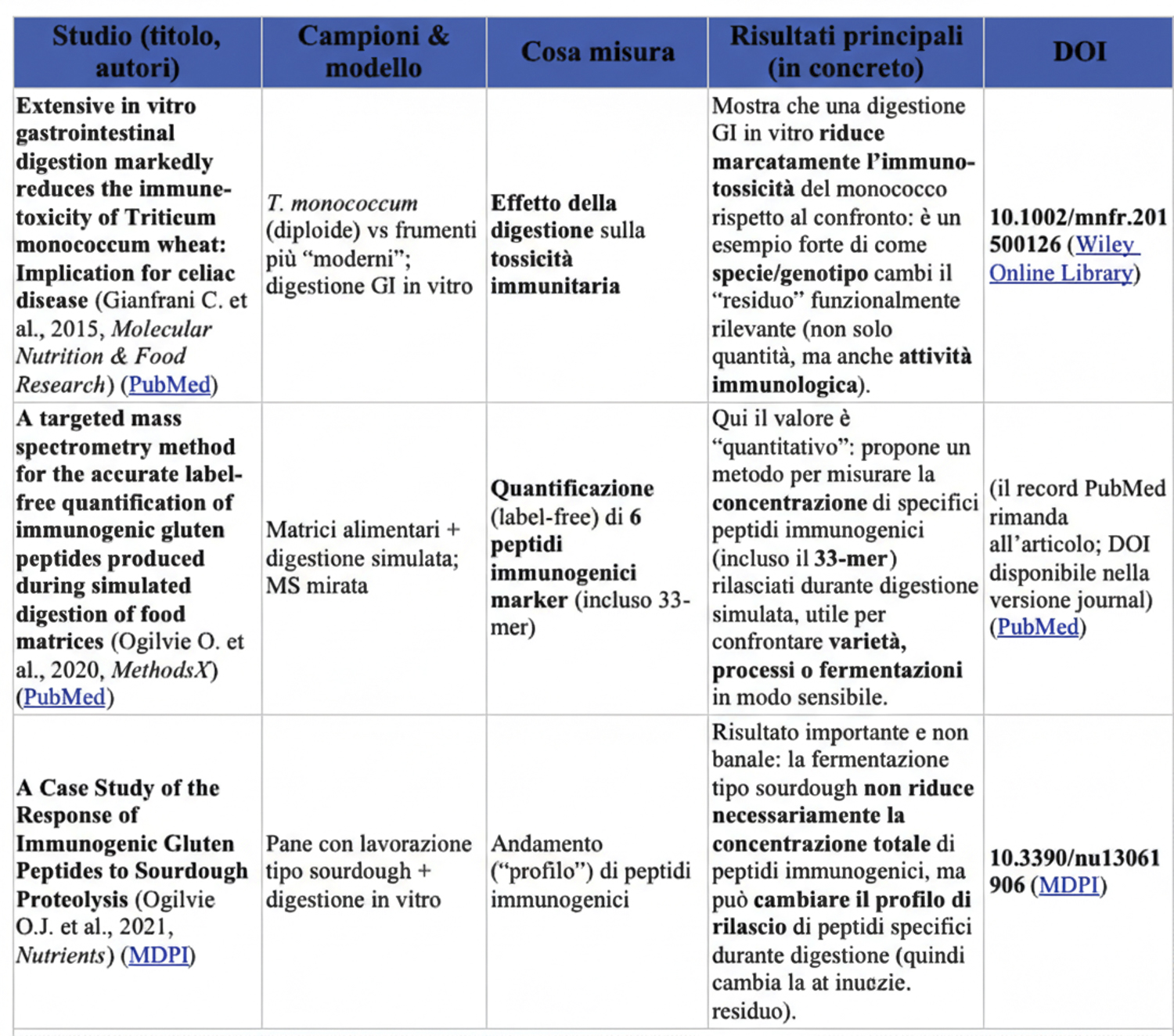
(approfondimento 2 di Potenziale genetico e condizioni di processo nella determinazione della forza del glutine, della digeribilità e dell’immunogenicità)
Il peptide 33-mer (sequenza LQLQPFPQPQLPYPQPQLPYPQPQLPYPQPQPF) è riconosciuto come uno dei peptidi più resistenti alla digestione gastro-intestinale derivati dalle proteine del glutine e come uno dei principali stimolatori delle cellule T nel contesto della celiachia.
La sua importanza deriva da tre caratteristiche chiave:
-
Resistenza enzimatica: la sua ricchezza in prolina e glutammina lo rende molto resistente agli enzimi digestivi umani (pepsina, tripsina, chimotripsina), permettendogli di persistere nel lume intestinale dopo la digestione in vitro e in vivo. (Nature)
-
Immunogenicità elevata: contiene diverse porzioni (epitopi) riconosciute dalle cellule T dei pazienti celiaci, ed è stato tra i primi peptide identificati con questa caratteristica. (PubMed)
-
Presenza nei frumenti più comuni: è presente nella maggior parte dei frumenti tetraploidi comuni (T. aestivum) e nella spelta, ma viene riportato assente nei tetraploidi/diploidi privi di D-genoma (come il grano duro, emmer e monococco). (ResearchGate)
Per questi motivi, il 33-mer è spesso utilizzato come marcatore per la valutazione della “immunogenicità da glutine” di farine/prodotti e per confrontare cultivar di frumento nell’ambito della ricerca sulla risposta immunitaria.
Risultati chiave degli studi sul 33-mer.
Shan et al. (2002) — Identificazione e immunogenicità del 33-mer.Titolo: A resistant peptide from gliadin that is a potent activator of intestinal T cells in celiac disease. Autori: Shan L., Molberg Ø., Parrot I., Hausch F., Filiz F., Gray G.M., Sollid L.M., Khosla C. Pubblicato in: Science (2002). DOI: 10.1126/science.1074624
Risultato fondamentale: questo lavoro classico ha isolato e caratterizzato il peptide 33-mer come uno dei più potenti attivatori di cellule T nei pazienti celiaci e ha dimostrato che è estremamente resistente alla digestione proteolitica standard, confermando la sua rilevanza immunogenica. (PubMed)
Vader et al. (2002) — Struttura e epitopi del 33-mer. Titolo: Structural basis for gluten intolerance in celiac sprue. Autori: Vader W., Stepniak D., Bunnik E., et al. Pubblicato in: Journal of Experimental Medicine (2002) DOI: 10.1084/jem.20020609
Risultato fondamentale: mappatura dei principali epitopi immunogenici presenti nelle gliadine, mostrando perché sequenze come il 33-mer — con epitopi multipli e sovrapposti — risultano così “attive” nel contesto immunitario. (d-nb.info).
Schalk et al. (2017) — Quantificazione e distribuzione del 33-mer nei frumenti. Titolo: Quantitation of the immunodominant 33-mer peptide from α-gliadin in wheat flours by liquid chromatography tandem mass spectrometry
Autori: Kathrin Schalk, Christina Lang, Herbert Wieser, Peter Koehler & Katharina Anne Scherf. Pubblicato in: Scientific Reports (2017) DOI: 10.1038/srep45092 (Nature). Questo studio ha misurato il contenuto del 33-mer in un ampio insieme di campioni di farine (moderne e antiche) usando un metodo mirato (SIDA + LC-MS/MS), contribuendo con dati importanti alla nostra comprensione della variabilità di questo peptide nello spettro dei genotipi di frumento.
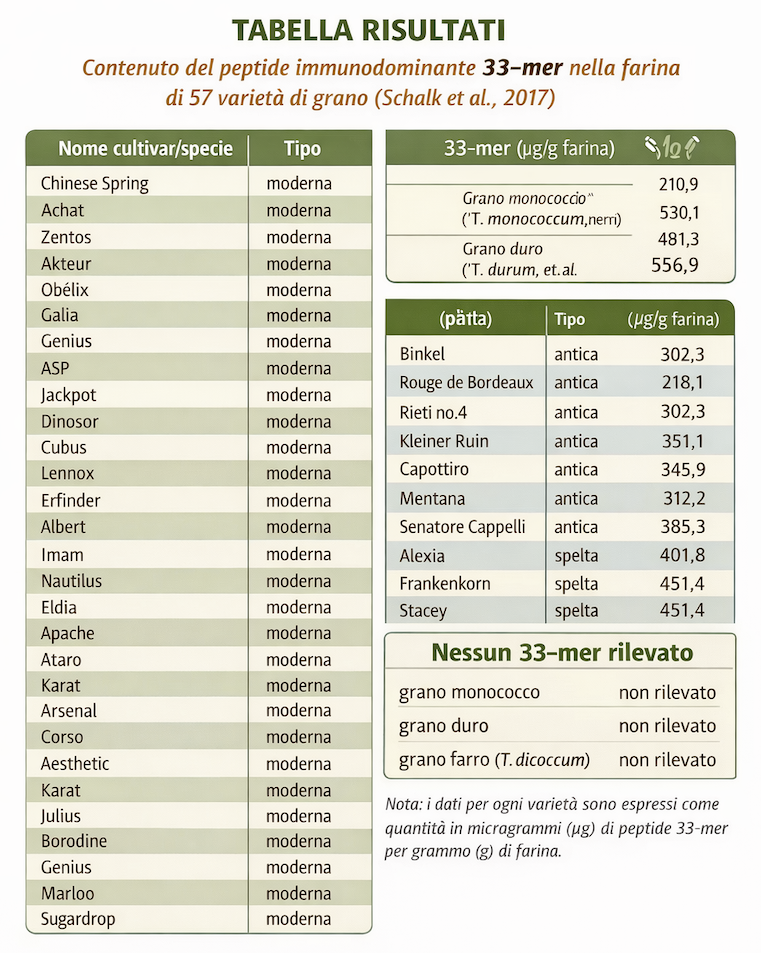
Risultati specifici da Schalk et al. (2017)
Panoramica generale:
-
Il 33-mer è stato rilevato in tutte le farine di frumento comune (hexaploide, Triticum aestivum) e spelta analizzate.
-
I valori rilevati variavano approssimativamente da 90,9 μg/g a 602,6 μg/g di farina.
-
Invece non è stato rilevato (< limite di rivelabilità) nei cereali privi del D-genoma come grano duro, emmer ed einkorn (monococco), coerente con l’assenza di α2-gliadine che codificano questo peptide. (ResearchGate)
Interpretazione: la variabilità osservata indica che, anche all’interno dei frumenti più “simili” dal punto di vista tassonomico, la quantità di peptide 33-mer può variare considerevolmente, suggerendo che genotipo e variazione di cultivar influiscono in modo concreto sul contenuto di peptidi immunogenici legati alla celiachia.
Altri studi collegati e complementarietà
✔ Norwig et al. (2024) — confermano come il 33-mer sia presente in tutti i frumenti comuni e spelta analizzati, rafforzando il valore del focus su questo peptide nella letteratura peptidomica legata al glutine. (ACS Publications)
✔ Approcci proteomici più ampi (peptidomica) mostrano che il 33-mer è solo uno dei peptidi immunogenici che possono persistere dopo digestione, ma rimane un marcatore robusto per confronto tra genotipi e processi tecnici (fermentazione, cottura, ecc.). (ScienceDirect)
Box esplicativo: risultati principali di Schalk et al. (2017)
Contenuto del peptide 33-mer (μg/g di farina) nei frumenti analizzati
Lo studio ha mostrato che il peptide 33-mer è presente in tutte le farine di frumento comune e spelta analizzate con i seguenti caratteristiche: (Nature)
-
Valore minimo osservato: ~90,9 μg/g di farina
-
Valore massimo osservato: ~602,6 μg/g di farina
-
Distribuzione: la maggior parte dei campioni si colloca nel range 200–400 μg/g
-
Assenza: il peptide non è stato rilevato in Triticum durum (grano duro), T. turgidum dicoccum (emmer) e T. monococcum (monococco), probabilmente per l’assenza dell’α2-gliadina D-genomica. (ResearchGate)
Perché questa sottosezione rende il quadro completo e leggibile
✅ Partendo da un concetto biologico chiaro (resistenza + immunogenicità), questa sottosezione collega:
-
meccanismi molecolari (epitopi multipli nel peptide),
-
evidenze sperimentali classiche,
-
dati quantitativi reali su cultivar diverse,
-
coerenza con la variabilità osservata in studi più ampi (peptidomica).
Questo fornisce al lettore un quadro solido per comprendere non solo che il 33-mer esiste, ma perché la sua presenza/quantità varia tra grani e perché conta per la digestione e la risposta immunitaria.