(Ruolo di lieviti, enzimi, batteri lattici e microbiota intestinale)
Indice generale
-
Struttura del glutine
-
Cos’è l’idrolisi del glutine
-
Il ruolo del lievito di birra
-
Enzimi naturalmente presenti nella farina
-
Processi biochimici nell’impasto
-
Fermentazione breve (4 ore) con lievito di birra
-
Fermentazione prolungata (12 ore) con lievito di birra
-
Perché la pasta madre è diversa
-
Microbiologia della pasta madre
-
Effetti della fermentazione lattica
-
Degradazione dei peptidi immunogenici del glutine
-
Riduzione dei FODMAP
-
Ruolo della temperatura nella fermentazione
-
Ruolo dell’idratazione dell’impasto
-
Differenza tra lievitazione e maturazione
-
Perché troppa idrolisi peggiora la struttura
-
Il ruolo della forza della farina (W)
-
Quanto glutine viene realmente idrolizzato negli studi
-
Digestione umana del glutine
-
Digeribilità reale e sensazione di leggerezza
-
Il mito delle maturazioni di 48–72 ore
-
Perché alcune pizze causano gonfiore
-
Ruolo del microbiota intestinale
-
Glutine o fruttani: cosa causa i sintomi
-
Riduzione dei FODMAP con pasta madre
-
Variabilità individuale nella digestione
-
Schema generale dei processi biochimici dell’impasto
-
Reazioni chimiche principali durante la fermentazione
-
Evoluzione della struttura dell’impasto durante la fermentazione
-
Percentuali di degradazione del glutine negli studi sperimentali
-
Conclusioni generali
-
Bibliografia
1. Struttura del glutine [1][3]
Il glutine è un complesso proteico presente nel frumento che si forma quando la farina viene idratata e sottoposta a impastamento. Le principali proteine coinvolte sono le gliadine e le glutenine, che appartengono alla classe delle prolamine di riserva del grano.
Le gliadine sono proteine monomeriche solubili in soluzioni idroalcoliche e sono principalmente responsabili della viscosità ed estensibilità dell’impasto.
Le glutenine, invece, sono proteine polimeriche costituite da subunità ad alto e basso peso molecolare (HMW-GS e LMW-GS) unite tra loro mediante legami disolfuro. Queste proteine conferiscono all’impasto elasticità e resistenza.
Durante l’impasto, le interazioni tra gliadine e glutenine portano alla formazione di una rete proteica tridimensionale viscoelastica, in grado di trattenere i gas prodotti durante la fermentazione e responsabile della struttura dei prodotti da forno [1].
Un ruolo fondamentale nella struttura del glutine è svolto dalle GMP (Glutenin Macropolymer), grandi aggregati di glutenine ad alto peso molecolare che costituiscono la frazione insolubile del glutine. Le GMP rappresentano l’ossatura strutturale della rete glutinica e sono fortemente correlate con la forza della farina, la tenacità dell’impasto e la qualità panificatoria [3].
La stabilità della rete glutinica dipende principalmente da diverse interazioni intermolecolari, tra cui:
-
legami disolfuro tra le subunità delle glutenine
-
legami idrogeno tra gruppi polari delle proteine
-
interazioni idrofobiche tra regioni non polari delle catene proteiche.
2. Cos’è l’idrolisi del glutine [2]
L’idrolisi consiste nella scissione dei legami peptidici delle proteine con formazione di peptidi di dimensioni più piccole.
Nel caso del glutine, il processo è catalizzato da enzimi proteolitici (proteasi), che utilizzano una molecola di acqua per rompere il legame peptidico della catena proteica.
In termini generali, la reazione può essere schematizzata come:
proteina + H₂O —(proteasi)→ peptidi più piccoli
L’idrolisi modifica la struttura della rete glutinica e le proprietà reologiche dell’impasto. In particolare:
Quando l’idrolisi è moderata:
-
aumenta l’estensibilità dell’impasto
-
migliora la lavorabilità
Quando l’idrolisi è eccessiva:
-
indebolisce la rete glutinica
-
riduce la capacità di trattenere i gas di fermentazione [2].
3. Il ruolo del lievito di birra [4]
Il Saccharomyces cerevisiae è responsabile della fermentazione alcolica.
Reazione metabolica: glucosio → CO₂ + etanolo.
Effetti:
-
crescita dell’impasto
-
sviluppo aromatico.
Il lievito produce quantità limitate di proteasi e quindi non contribuisce significativamente alla degradazione del glutine [4].
4. Enzimi naturalmente presenti nella farina [4][5]
La farina contiene diversi enzimi endogeni che svolgono un ruolo fondamentale nelle trasformazioni biochimiche che avvengono durante l’impasto e la fermentazione. Questi enzimi contribuiscono alla degradazione controllata delle principali macromolecole della farina, in particolare amidi e proteine.
Tra gli enzimi più importanti si trovano le amilasi, che catalizzano la degradazione dell’amido. In particolare, l’amido viene progressivamente idrolizzato secondo la sequenza:
amido → maltosio → glucosio
Gli zuccheri semplici prodotti rappresentano una fonte di energia per i lieviti, che li utilizzano nel metabolismo fermentativo per produrre anidride carbonica (CO₂) ed altri metaboliti coinvolti nello sviluppo dell’impasto [4].
Un altro gruppo di enzimi importanti è rappresentato dalle proteasi, che agiscono sulle proteine del glutine. Questi enzimi idrolizzano progressivamente le catene proteiche secondo il processo:
glutine → polipeptidi → peptidi
Questa degradazione parziale delle proteine modifica la struttura della rete glutinica, rendendo l’impasto più estensibile e lavorabile.
Nel loro insieme, le reazioni catalizzate da amilasi e proteasi contribuiscono ai processi di maturazione enzimatica dell’impasto, che influenzano la struttura, la fermentabilità e le caratteristiche finali del prodotto da forno [5].
5. Processi biochimici nell’impasto [4][5]
Quando farina e acqua vengono mescolate, si attivano una serie di processi fisici, chimici e microbiologici che determinano l’evoluzione dell’impasto nel tempo. In particolare, si attivano tre principali sistemi interconnessi:
-
formazione della rete glutinica
-
attività enzimatica della farina
-
fermentazione microbica
L’idratazione della farina permette alle proteine del glutine (gliadine e glutenine) di assorbire acqua e di interagire tra loro, formando progressivamente una rete proteica tridimensionale che conferisce all’impasto elasticità ed estensibilità.
Parallelamente si attivano gli enzimi naturalmente presenti nella farina, come amilasi e proteasi, che iniziano a degradare rispettivamente amidi e proteine, contribuendo ai processi di maturazione dell’impasto.
Infine, i lieviti e gli eventuali batteri lattici presenti nell’impasto metabolizzano gli zuccheri disponibili producendo anidride carbonica (CO₂) e altri metaboliti, responsabili dell’aumento di volume dell’impasto e dello sviluppo di composti aromatici.
In condizioni normali, i processi nell’impasto seguono una sequenza tipica:
-
idratazione delle proteine e formazione iniziale della rete glutinica
-
attività delle amilasi, con degradazione dell’amido e produzione di zuccheri fermentescibili
-
fermentazione dei lieviti, con produzione di CO₂
-
maturazione enzimatica, che modifica progressivamente la struttura di amidi e proteine.
Questi processi avvengono in modo simultaneo e interdipendente, influenzando la struttura dell’impasto, la sua lavorabilità e le caratteristiche del prodotto finale.
6. Fermentazione breve (circa 4 ore) [6]
Durante una fermentazione breve, come nei processi di panificazione con tempi ridotti, l’attività predominante è quella dei lieviti, che metabolizzano gli zuccheri disponibili producendo anidride carbonica (CO₂) ed etanolo. La CO₂ rimane intrappolata nella rete glutinica e provoca l’aumento di volume dell’impasto.
In queste condizioni il tempo a disposizione per i processi di maturazione enzimatica è limitato. Di conseguenza, gli enzimi presenti nella farina, in particolare le proteasi, hanno poco tempo per agire sulle proteine del glutine.
Il risultato è che:
-
l’idrolisi delle proteine del glutine rimane molto limitata
-
la struttura della rete glutinica subisce poche modificazioni
-
l’impasto mantiene una struttura proteica relativamente compatta e poco modificata [6].
7. Fermentazione prolungata (circa 12 ore) [5]
Durante fermentazioni più lunghe, l’impasto rimane per un tempo maggiore sotto l’azione combinata di enzimi e microrganismi, permettendo lo sviluppo più completo dei processi di maturazione. In particolare, le proteasi presenti nella farina iniziano a idrolizzare alcune catene delle proteine del glutine, rompendo parzialmente i legami peptidici. Questo processo porta a una riduzione della rigidità della rete glutinica e rende l’impasto più estensibile e lavorabile.
Contemporaneamente, le amilasi continuano a degradare l’amido producendo zuccheri più semplici, che possono essere utilizzati dai lieviti nel processo fermentativo. Durante la fermentazione si osserva inoltre una leggera diminuzione del pH dell’impasto, dovuta alla produzione di acidi organici da parte dei microrganismi. Questo abbassamento del pH può favorire l’attività di alcuni enzimi, contribuendo ulteriormente ai processi di maturazione enzimatica dell’impasto [5].
8. Perché la pasta madre è diversa [5][8]
La pasta madre contiene:
-
lieviti
-
batteri lattici.
I batteri lattici producono:
-
acido lattico
-
acido acetico.
Questa acidificazione aumenta l’attività delle proteasi e la degradazione del glutine [5].
Alcuni batteri lattici possiedono sistemi proteolitici complessi, comprendenti enzimi come prolil endopeptidasi ed endopeptidasi specifiche per residui di prolina, che sono in grado di degradare ulteriormente i peptidi ricchi in prolina, inclusi alcuni frammenti immunogenici del glutine.
Tra i microrganismi maggiormente studiati per questa attività si trovano specie appartenenti ai generi Lactobacillus, Lactiplantibacillus e Lacticaseibacillus, tra cui:
-
Lactobacillus sanfranciscensis
-
Lactobacillus plantarum (oggi Lactiplantibacillus plantarum)
-
Lactobacillus brevis
-
Lactobacillus helveticus
-
Lactobacillus paracasei
Questi microrganismi, spesso presenti nei lieviti madre, possiedono sistemi proteolitici in grado di idrolizzare peptidi ricchi in prolina e contribuire alla degradazione di sequenze immunogeniche della gliadina, inclusi frammenti derivati dal peptide 33-mer, riducendone il potenziale immunogenico [8].
9. Microbiologia della pasta madre [7]
La pasta madre ospita una comunità microbica complessa e relativamente stabile, composta principalmente da lieviti e batteri lattici, che convivono in un sistema di fermentazione naturale. L’equilibrio tra questi microrganismi dipende da diversi fattori, tra cui tipo di farina, idratazione dell’impasto, temperatura e modalità di rinfresco.
Tra i lieviti più frequentemente associati alla pasta madre si trovano:
-
Saccharomyces cerevisiae
-
Candida milleri (oggi spesso classificata come Kazachstania humilis)
Questi microrganismi sono responsabili principalmente della produzione di anidride carbonica (CO₂) attraverso la fermentazione degli zuccheri, contribuendo all’aumento di volume dell’impasto.
Accanto ai lieviti, la pasta madre contiene numerosi batteri lattici, tra cui:
-
Lactobacillus sanfranciscensis
-
Lactobacillus plantarum
-
Lactobacillus brevis
I batteri lattici metabolizzano gli zuccheri producendo acido lattico e acido acetico, contribuendo allo sviluppo dell’acidità dell’impasto e alla formazione di composti aromatici caratteristici della fermentazione naturale [7].
10. Effetti della fermentazione lattica [5][7]
La fermentazione lattica svolge un ruolo importante nell’evoluzione biochimica dell’impasto durante la fermentazione con pasta madre.
Uno degli effetti principali è la progressiva acidificazione dell’impasto, dovuta alla produzione di acido lattico e acido acetico da parte dei batteri lattici. La diminuzione del pH influenza diversi processi biochimici e tecnologici. In particolare, l’acidificazione può favorire una maggiore attività di alcuni enzimi presenti nella farina, come amilasi e proteasi, contribuendo ai processi di maturazione enzimatica dell’impasto. Inoltre, la presenza di batteri lattici e dei loro sistemi proteolitici può portare a una maggiore degradazione delle proteine, inclusa una parziale idrolisi delle proteine del glutine. Questo processo può modificare la struttura della rete proteica, rendendo l’impasto più estensibile e lavorabile. Nel complesso, la fermentazione lattica contribuisce non solo allo sviluppo dell’acidità, ma anche alla formazione di aromi, alla modifica della struttura dell’impasto e alle caratteristiche finali del prodotto da forno.
11. Degradazione dei peptidi immunogenici [8]
Durante la digestione gastrointestinale, le proteine del glutine vengono parzialmente idrolizzate da enzimi digestivi come pepsina, tripsina e chimotripsina. Tuttavia, a causa dell’elevato contenuto di prolina e glutammina, alcune sequenze peptidiche risultano particolarmente resistenti alla degradazione enzimatica.
Questa resistenza alla digestione è dovuta in gran parte all’elevato contenuto di residui di prolina nelle proteine del glutine, che rende molti legami peptidici poco accessibili agli enzimi digestivi umani.
Tra questi frammenti, alcuni peptidi sono immunogenici, cioè in grado di attivare la risposta immunitaria nei soggetti affetti da celiachia. Uno dei più studiati è il peptide 33-mer derivato dalla α-gliadina, noto per la sua elevata resistenza alla digestione e per la presenza di diversi epitopi riconosciuti dal sistema immunitario. La sua resistenza deriva dall’elevato contenuto di prolina e glutammina, che rende il peptide poco suscettibile agli enzimi digestivi umani.
Oltre ai peptidi immunogenici, durante la digestione del glutine si formano anche peptidi resistenti ma non immunogenici, che non sono in grado di attivare la risposta immunitaria tipica della celiachia. Questi frammenti derivano dalla degradazione parziale delle proteine del glutine e possono persistere nel tratto gastrointestinale.
In individui con alterazioni della funzionalità gastrointestinale, come nel caso di una barriera intestinale compromessa o di disbiosi del microbiota, tali peptidi possono contribuire a effetti biologici indesiderati. In particolare, alcuni studi suggeriscono che essi possano interagire con il microbiota intestinale, influenzare la permeabilità della barriera epiteliale e modulare, seppur indirettamente, alcune risposte immunitarie locali.
Anche i peptidi indigeriti non immunogenici possono persistere nel lume intestinale e partecipare ai processi di fermentazione microbica o interagire con il microbiota. Pur non attivando la risposta immunitaria tipica della celiachia, la loro presenza può contribuire, in soggetti predisposti, alla comparsa di sintomi gastrointestinali o a una sensazione di ridotta digeribilità.
12. Riduzione dei FODMAP e modificazione di altri composti del grano [9]
Il grano contiene fruttani, carboidrati appartenenti alla categoria dei FODMAP (Fermentable Oligo-, Di-, Monosaccharides and Polyols). Questi composti possono essere scarsamente digeriti nell’intestino tenue e fermentati dal microbiota intestinale, causando sintomi gastrointestinali in individui sensibili. Durante la fermentazione lattica, alcuni microrganismi sono in grado di metabolizzare i fruttani attraverso enzimi come le fruttanasi, convertendoli in zuccheri più semplici che vengono successivamente trasformati in acidi organici (principalmente acido lattico e acido acetico):
fruttani → zuccheri semplici → acidi organici
Questo processo può portare a una riduzione significativa del contenuto di FODMAP nel pane, in particolare nei prodotti ottenuti con fermentazioni prolungate, come nel caso del lievito madre [9].
Oltre ai fruttani, il grano contiene anche le ATI (Amylase–Trypsin Inhibitors), un gruppo di proteine coinvolte nei meccanismi di difesa della pianta. Alcuni studi suggeriscono che i processi di fermentazione, in particolare quelli mediati da batteri lattici, possano ridurre o modificare parzialmente queste proteine, contribuendo potenzialmente a una migliore tollerabilità del prodotto finale [5].
13. Ruolo della temperatura [4]
La temperatura è uno dei fattori principali che influenzano la velocità e l’equilibrio dei processi che avvengono nell’impasto, in particolare fermentazione microbica e attività enzimatica.
A temperature più elevate, l’attività metabolica dei lieviti e dei batteri aumenta, determinando una fermentazione più rapida e una produzione più veloce di CO₂. Tuttavia, una fermentazione troppo veloce può ridurre il tempo disponibile per i processi di maturazione enzimatica, con una minore degradazione di amidi e proteine.
Al contrario, a temperature più basse la fermentazione avviene più lentamente. Questo rallentamento dell’attività microbica permette agli enzimi presenti nella farina (come amilasi e proteasi) di agire più a lungo sull’impasto, favorendo una maggiore maturazione enzimatica.
Di conseguenza:
-
temperature alte → fermentazione veloce e tempi più brevi di lavorazione;
-
temperature basse → fermentazione più lenta e maggiore sviluppo dei processi di maturazione.
Per questo motivo, nelle tecniche di panificazione moderna si utilizzano spesso fermentazioni controllate a bassa temperatura, che permettono di gestire meglio i tempi di produzione e di favorire lo sviluppo di struttura, aromi e caratteristiche reologiche dell’impasto.
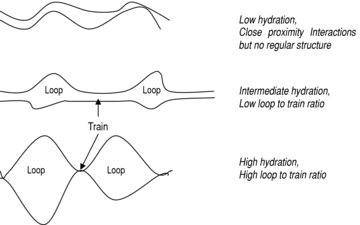
14. Ruolo dell’idratazione [5]
L’idratazione dell’impasto, cioè la quantità di acqua presente rispetto alla farina, rappresenta un fattore fondamentale nei processi che avvengono durante l’impasto e la fermentazione.
L’acqua svolge diverse funzioni tecnologiche e biochimiche, tra cui:
-
favorire la mobilità molecolare dei componenti dell’impasto
-
permettere lo sviluppo della rete glutinica attraverso l’idratazione delle proteine del glutine
-
facilitare l’attività degli enzimi presenti nella farina e prodotti dai microrganismi.
Un’adeguata disponibilità di acqua consente agli enzimi, come amilasi e proteasi, di agire più efficacemente su amidi e proteine, favorendo i processi di maturazione dell’impasto.
Gli impasti più idratati tendono quindi a presentare una maggiore attività enzimatica e una struttura più estensibile, permettendo una maturazione più efficace nel corso della fermentazione. Inoltre, una maggiore idratazione può favorire la formazione di una struttura più alveolata nel prodotto finale.
Al contrario, impasti con bassa idratazione risultano generalmente più compatti e limitano la mobilità delle molecole e l’attività enzimatica, riducendo in parte l’intensità dei processi di maturazione [5].