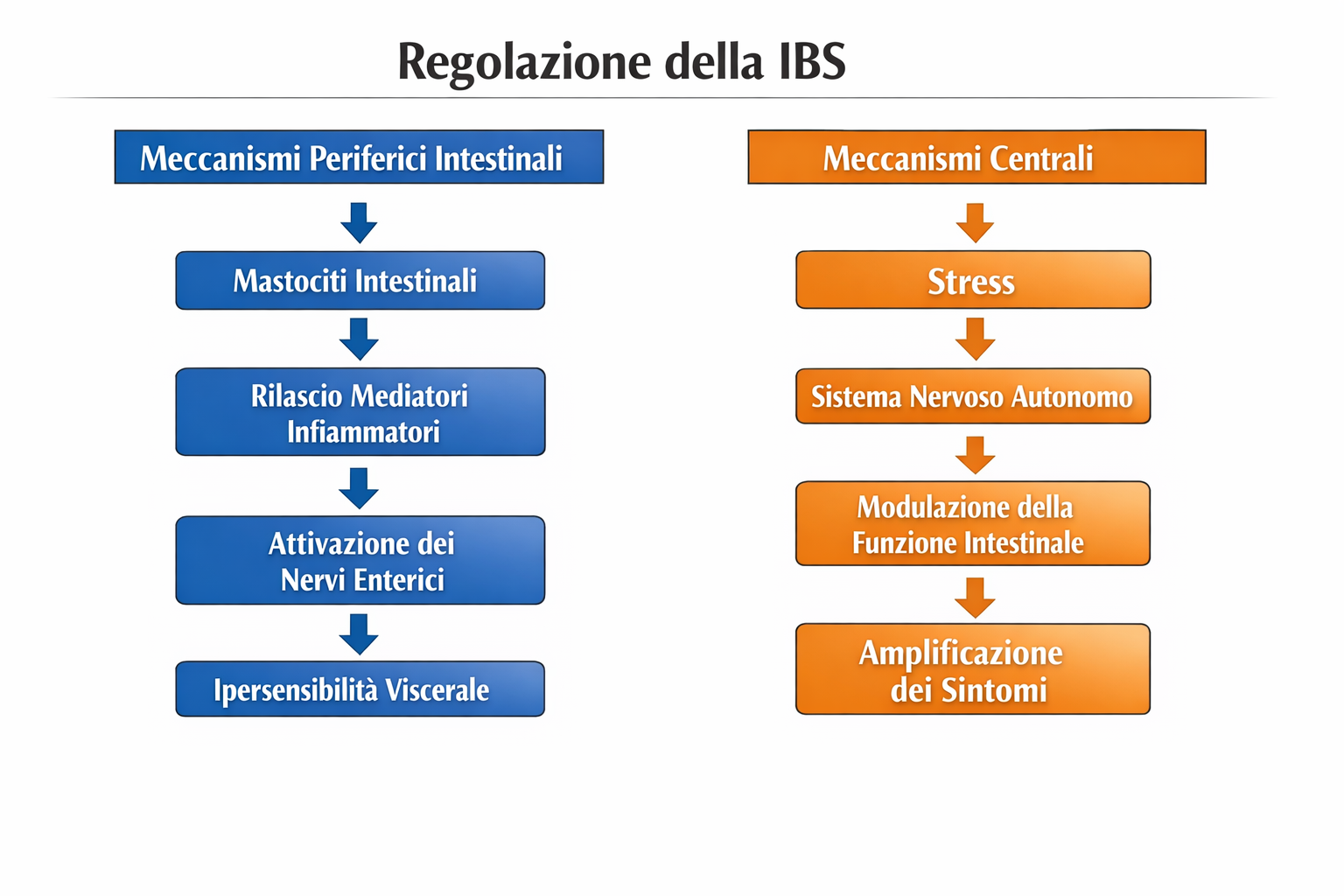
Non sempre è facile gestire stress e ansia. Se la tensione è temporanea – per esempio prima di un esame o di una scadenza – il problema tende a risolversi spontaneamente quando la situazione termina.Più difficile è quando lo stress diventa prolungato, come accade spesso in contesti lavorativi difficili o in situazioni familiari complesse. In questi casi il supporto di uno psicologo può essere molto utile.Tuttavia esistono alcune strategie di auto-gestione dello stress che derivano dalle tecniche utilizzate in psicologia e che possono rappresentare un primo livello di intervento.
1. Riconoscere i segnali dello stress
Il primo passo è imparare a riconoscere i segnali che il corpo invia quando lo stress aumenta.
I segnali più comuni sono:
-
tensione muscolare
-
respiro corto o affannoso
-
irritabilità
-
difficoltà di concentrazione
-
disturbi intestinali o digestivi.
Prendere consapevolezza di questi segnali permette di intervenire prima che lo stress diventi troppo intenso.
2. Regolare la respirazione
Molte tecniche psicologiche utilizzano esercizi di respirazione lenta e controllata.
Un esercizio semplice consiste nel:
-
inspirare lentamente per circa 4 secondi
-
trattenere il respiro per 1-2 secondi
-
espirare lentamente per 6 secondi.
Ripetere questo ciclo per alcuni minuti aiuta a ridurre l’attivazione del sistema nervoso simpatico, favorendo la risposta di rilassamento.
3. Ridurre il “rumore mentale”
Una delle principali fonti di ansia è il continuo flusso di pensieri preoccupanti che si ripresentano nella mente. Questo fenomeno è spesso definito ruminazione mentale: una sorta di dialogo interno ripetitivo in cui la mente continua a ripercorrere problemi, timori o scenari negativi senza arrivare a una soluzione concreta.
Quando questo processo diventa persistente, il cervello rimane in uno stato di attivazione continua, che può mantenere attiva anche la risposta fisiologica allo stress. In queste condizioni l’organismo produce più facilmente ormoni dello stress, come il cortisolo, e il sistema nervoso simpatico rimane più attivo. Questo stato può influenzare anche l’intestino, aumentando la sensibilità viscerale e favorendo sintomi come tensione addominale, gonfiore o alterazioni della motilità intestinale.
Una tecnica semplice, utilizzata anche in alcuni approcci della terapia cognitivo-comportamentale, consiste nel mettere per iscritto le preoccupazioni. Scrivere i pensieri su carta o su un taccuino permette di “spostarli” dalla mente a uno spazio esterno, rendendoli più concreti e meno opprimenti.
Questo esercizio può aiutare a:
-
chiarire le situazioni, trasformando pensieri vaghi in problemi più definiti
-
ridurre la ruminazione mentale, interrompendo il ciclo dei pensieri ripetitivi
-
distinguere ciò che è sotto il proprio controllo da ciò che non lo è
-
individuare possibili azioni pratiche per affrontare i problemi reali.
Un metodo utile consiste nel dividere la pagina in due colonne: nella prima si scrivono le preoccupazioni, nella seconda si indicano eventuali azioni possibili o, se il problema non è controllabile, si prende semplicemente atto della situazione.
Anche dedicare ogni giorno qualche minuto a questo esercizio può aiutare a ridurre il sovraccarico mentale e favorire uno stato di maggiore calma. Riducendo il livello di tensione psicologica si contribuisce indirettamente anche a riequilibrare l’asse cervello-intestino, limitando gli effetti dello stress sulla funzione digestiva.
Comprendere il comportamento dell’altro
Una parte significativa dello stress quotidiano deriva da situazioni conflittuali, soprattutto in ambito lavorativo o familiare. In questi contesti il disagio nasce spesso dall’interpretazione immediata del comportamento dell’altra persona: il cervello tende infatti a formulare rapidamente spiegazioni negative (“lo fa apposta”, “non mi rispetta”, “vuole mettermi in difficoltà”).
In realtà, non sempre l’aggressività o l’irritazione dell’altro nasce da un’intenzione ostile. In molti casi può essere la manifestazione di una forte preoccupazione o di una difficoltà personale che la persona non riesce a gestire o a esprimere in modo costruttivo. Quando qualcuno si sente sotto pressione, preoccupato o incapace di trovare una soluzione a un problema, può reagire con irritazione, rigidità o aggressività.
Riconoscere questa possibilità non significa giustificare il comportamento dell’altro, ma può aiutare a ridurre la reazione emotiva immediata e a osservare la situazione con maggiore lucidità.
Una strategia utilizzata in diversi approcci psicologici consiste proprio nel analizzare il comportamento dell’altra persona cercando di comprenderne le possibili motivazioni. L’obiettivo non è giustificare il comportamento, ma ampliare la prospettiva e ridurre il conflitto emotivo.
Può essere utile chiedersi, ad esempio:
-
Quali pressioni o difficoltà potrebbe avere l’altra persona?
-
Sta reagendo a una situazione di stress o preoccupazione?
-
Potrebbe aver interpretato male qualcosa che ho detto o fatto?
Questo esercizio di cambio di prospettiva può avere diversi effetti positivi:
-
riduce la tendenza alla ruminazione mentale
-
diminuisce la risposta emotiva immediata allo stress
-
aiuta a individuare modalità più costruttive di affrontare il conflitto.
Comprendere meglio le motivazioni dell’altro può anche permettere di formulare risposte più efficaci, proponendo soluzioni o punti di vista alternativi che favoriscano una comunicazione più equilibrata. In molti casi questo semplice cambiamento di prospettiva riduce il livello di tensione psicologica e contribuisce indirettamente a riequilibrare la risposta allo stress dell’organismo.
Una tecnica semplice in tre passaggi per affrontare i conflitti
Quando una situazione conflittuale provoca stress o ansia, può essere utile fermarsi per qualche minuto e seguire tre passaggi molto semplici.
1. Fermarsi e ridurre la reazione immediata
Il primo passo consiste nel evitare una risposta impulsiva. Quando una persona reagisce con aggressività o irritazione, il nostro cervello tende a rispondere nello stesso modo, alimentando il conflitto.
Fare una breve pausa – anche solo respirare lentamente per qualche secondo – permette di ridurre l’attivazione emotiva e di evitare risposte che potrebbero peggiorare la situazione.
2. Cercare di capire cosa potrebbe preoccupare l’altra persona
Il secondo passo è provare a considerare quale problema o preoccupazione possa esserci dietro il comportamento dell’altro.
Domande utili possono essere:
-
Quale difficoltà potrebbe trovarsi ad affrontare questa persona?
-
Sta reagendo a una pressione lavorativa o personale?
-
Potrebbe sentirsi insicura o sotto attacco?
Questo passaggio non serve a giustificare il comportamento, ma a ridurre la percezione di ostilità e a comprendere meglio il contesto.
3. Spostare la conversazione verso il problema, non verso la persona
Il terzo passo consiste nel riportare la discussione sul problema concreto, evitando di trasformarla in uno scontro personale.
Ad esempio si può dire:
-
“Cerchiamo di capire insieme come risolvere questa situazione.”
-
“Vediamo se troviamo una soluzione che funzioni per entrambi.”
Questo tipo di approccio aiuta a trasformare il conflitto da uno scontro emotivo a un tentativo condiviso di soluzione.
Perché questa strategia riduce lo stress
Quando si riesce a interrompere il ciclo di reazioni impulsive, il cervello riduce l’attivazione della risposta allo stress. Questo contribuisce a riequilibrare anche il funzionamento dell’asse cervello–intestino, limitando gli effetti dello stress sull’organismo e sui disturbi digestivi. In altre parole, imparare a gestire meglio i conflitti quotidiani non aiuta solo il benessere psicologico, ma può avere effetti positivi anche sulla salute dell’intestino.
4. Introdurre pause di recupero durante la giornata
Lo stress cronico spesso deriva da periodi prolungati senza pause.
Molti psicologi suggeriscono di introdurre brevi pause di recupero durante la giornata, anche di pochi minuti, per esempio:
-
una breve camminata
-
qualche minuto di respirazione lenta
-
allontanarsi temporaneamente da schermi e stimoli.
Queste pause aiutano a ridurre l’attivazione fisiologica dello stress.
5. Attività fisica regolare
L’attività fisica è uno degli strumenti più efficaci per ridurre lo stress.
Il movimento:
-
riduce i livelli di cortisolo
-
aumenta la produzione di endorfine
-
migliora la regolazione dell’umore.
Non è necessario svolgere attività intense: anche camminare 20-30 minuti al giorno può avere effetti significativi.
6. Curare il ritmo sonno-veglia
Lo stress cronico spesso peggiora quando il sonno è insufficiente o irregolare.
Alcune regole utili includono:
-
mantenere orari di sonno regolari
-
ridurre l’esposizione a schermi luminosi prima di dormire
-
evitare stimolanti nelle ore serali.
Il sonno adeguato aiuta il cervello a regolare meglio la risposta allo stress.
7. Quando chiedere aiuto
Se stress e ansia persistono nel tempo e iniziano a interferire con la qualità della vita, è importante considerare il supporto di uno psicologo o psicoterapeuta. Le tecniche professionali, come la terapia cognitivo-comportamentale o la mindfulness clinica, possono aiutare a sviluppare strategie più profonde per gestire lo stress cronico.
✔ In molti casi piccoli cambiamenti nelle abitudini quotidiane possono già migliorare l’equilibrio tra cervello e intestino, contribuendo a ridurre i sintomi legati allo stress.
Box – 7 segnali che indicano che lo stress sta influenzando l’intestino
|
Segnale |
Cosa succede |
|---|---|
|
1. Gonfiore addominale frequente |
Lo stress aumenta la sensibilità intestinale e può amplificare la percezione della distensione addominale. |
|
2. Alterazioni dell’alvo |
Possono comparire diarrea, stipsi o alternanza delle due condizioni. |
|
3. Dolore addominale ricorrente |
L’ipersensibilità dei nervi intestinali rende più dolorosi stimoli normalmente innocui. |
|
4. Urgenza di andare in bagno |
Lo stress può accelerare la motilità del colon attraverso il sistema nervoso autonomo. |
|
5. Sensazione di “nodo allo stomaco” |
L’attivazione della risposta allo stress modifica la motilità gastrica e intestinale. |
|
6. Peggioramento dei sintomi nei periodi di tensione |
I sintomi intestinali tendono ad aumentare durante periodi di ansia o pressione emotiva. |
|
7. Miglioramento nei periodi di relax |
Quando lo stress diminuisce, spesso anche i disturbi intestinali si riducono. |
✔ Messaggio chiave:
quando questi segnali compaiono o peggiorano in periodi di forte tensione, è possibile che il disturbo sia legato all’asse cervello–intestino, cioè al modo in cui lo stress influenza la funzione intestinale.
Box – 5 abitudini quotidiane che proteggono l’asse cervello–intestino
|
Abitudine |
Perché è utile |
|---|---|
|
1. Dormire a orari regolari |
Il sonno stabilizza il sistema nervoso e riduce i livelli di cortisolo, l’ormone dello stress. |
|
2. Fare attività fisica moderata |
Camminare o fare esercizio regolare riduce lo stress e migliora la motilità intestinale. |
|
3. Mangiare con calma e in modo consapevole |
Consumare i pasti lentamente favorisce una digestione più efficiente e riduce la distensione intestinale. Quando si mangia troppo velocemente si tende a ingerire più aria (aerofagia) e a sovraccaricare temporaneamente il sistema digestivo, favorendo gonfiore e disagio addominale. Mangiare con calma permette invece di attivare meglio la fase digestiva regolata dal sistema nervoso parasimpatico, spesso definita risposta “rest and digest”. Masticare adeguatamente gli alimenti, fare piccole pause durante il pasto e prestare attenzione ai segnali di sazietà aiuta anche a migliorare la comunicazione tra intestino e cervello, riducendo il rischio di disturbi digestivi legati allo stress. |
|
4. Prendersi pause durante la giornata |
Brevi pause riducono l’attivazione del sistema nervoso simpatico e favoriscono il rilassamento. |
|
5. Ridurre il sovraccarico mentale |
Tecniche di respirazione, mindfulness o semplici momenti di relax aiutano a riequilibrare il dialogo tra cervello e intestino. |
✔ Messaggio finale
L’intestino e il cervello sono strettamente collegati. Prendersi cura dello stress quotidiano non significa solo migliorare il benessere mentale, ma anche proteggere l’equilibrio dell’intestino e prevenire molti disturbi digestivi.